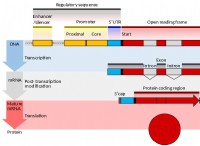
조정 화학에서 리간드는 루이스 염기로서 작용하고 금속의 빈 하이브리드 궤도에 전자 밀도를 기증하는 분자 또는 이온이다. 그것들은 금속과 함께 공유 결합을 형성합니다. 리간드는 치아, 전하 및 전계 강도에 따라 다양한 유형으로 분류 될 수 있습니다. 그것들은 너무 중요하여, 또한 자성 특성, 기하학 및 배위 화합물의 색상을 결정합니다. ‘리간드’라는 단어는 라틴어에서 유래하며‘바인딩’을 의미합니다. 그것은 금속 센터와 결합하고 조정 화합물을 형성합니다.
리간드 의미
리간드 위에서 지정된 바와 같이, 전자 밀도는 금속 이온에 기증한다. 이 정의에 의해, 리간드는 고독한 전자 쌍 또는 음전하를 가져야한다는 것은 분명합니다. 이를 바탕으로 리간드는 두 가지 유형 - 중성 및 음이온 성이 될 수 있습니다.
음이온 성 리간드는 음전하가있는 리간드입니다. 분자 이온 또는 원자 이온이있을 수 있습니다.
분자 음이온은 하나 이상의 유형의 원소로 구성됩니다.
-
예는 수산화물, 시안화물, 티오 시아 나이트, 질산염, 황산염, 아세테이트 등입니다.
가장 중요한 음이온 성 리간드의 전하와 이름을 아는 것이 중요합니다.
| anion
. | Symbol
| Charge
|
|
| h-
| -1
. |
|
| cl-
. | -1
. |
|
| f-
. | -1
. |
|
| br-
. | -1
. |
|
| i-
. | -1
. |
|
| |
| |
| -3
. |
|
| cn–
| -1
. |
|
| nc–
| -1
. |
|
| so42-
| | | s2o32-
| | -1
. |
|
| -1
. |
|
| -1
. |
| isothiocanate
| -1
. |
|
| c2o42-
| |
| CH3COO –
| -1
. |
중성 리간드는 금속에 기증 할 수있는 고독한 전자 쌍을 가지고 있습니다. 가장 일반적인 예는 다음과 같습니다.
- 물 (H2O)
- 암모니아 (NH3)
- Carbalyl (Co)
- 니트로 실 (NO)
- 메틸 아민 (CH3NH2)
- 트리 페닐 포스 핀 (PPH3)
치열
리간드와 관련된 가장 중요한 개념 중 하나는 치아의 개념입니다. 치아는 리간드에 존재하는 공여자 부위의 수로 정의된다. Halides의 예를 들어 봅시다. 그것들은 그룹 17 요소의 음이온입니다. 하나의 할라이드 이온은 모든 금속과 하나의 방식으로 만 결합 할 수 있습니다.
리간드는 치열에 따라 분류 될 수 있습니다 :
-
미확인 리간드 :리간드에 공여자 부위가 하나만있는 경우이를 미시성이라고합니다. 예는 cl-, nh3 등입니다.
-
다원자 리간드 :리간드에 하나 이상의 공여자 사이트/그룹이있는 경우 다중 소문이라고합니다. 다중 소문 리간드는 킬레이트 효과를 나타냅니다. 기증자 사이트의 수에 따라 다음 유형으로 나눌 수 있습니다.
-
Bidentate Ligand :두 개의 기증자 사이트가 있으며 둘 다 결합 형성에 동시에 참여할 수 있습니다. 에틸렌 디아민은 2 개의 질소 원자가 전자를 금속 중심에 동시에 기증 할 수있는 바 디테이트의 예이다.
-
템플릿 및 4 인치 리간드에는 각각 3 개 및 4 개의 공여자 부위가 있습니다. 디 에틸 렌트 리아민은 전자를 기증 할 수있는 3 개의 니트로겐을 갖는 삼지의 리간드이다. 트리 에틸렌 테트라민은 4 개의 니트로겐을 갖는 사면체 리간드이다.
-
16 진수 :6 개의 기증자 사이트가 있습니다. 예 :EDTA
hapticity
리간드의 햅틱은 일련의 연속 원자를 통해 금속 중심과 결합 리간드로 정의된다. 다수의 원자는 Pi- 결합 상호 작용을 통해 금속과 조정될 수있다. 햅틱을 나타내는 리간드는 사이클로 펜타 디에닐 음이온, 벤젠 등입니다. 그것은 그리스 상징으로 표시됩니다. 주어진 유형에서 금속과 조정 된 원자의 수는이 기호의 오른쪽 상단에 기록됩니다.
예를 들어, 벤젠의 2 개의 원자 만 금속과 조정되는 경우,이를 𝞰2- 벤젠이라고합니다. 4 개의 원자가 조정되면 𝞰4- 벤젠.
이러한 배위 화합물의 예 :Ferrocene (철은 2 개의 사이클로 펜타 디에닐 고리와 결합), Nickelocene 등
결론
리간드는 중앙 금속 이온과 결합하여 전자 밀도를 빈 궤도에 기증 할 수있는 루이스 염기입니다. 치열에 따라 다양한 유형으로 분류 할 수 있습니다. 그것들은 미확인, 다중 소문, 앰비던트 또는 폴리 덴테이트 일 수 있습니다. 다중 소문 리간드는 킬레이트 효과를 나타내며, 이는 조정 복합체의 안정성을 증가시킨다.
따라서이 화합물의 유효 원자 수는 36이며, 이는 크립톤의 원자 수 (36)와 같습니다.