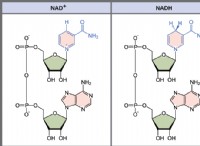
많은 다른 기능 그룹 중에서 아미드는 질소, 수소 또는 단일 결합에 의해 연결된 카르 보닐 그룹이다. 아민과 암모니아는 질소 함유 화합물이며 아미드는 암모니아 범주에 속합니다. 산의 히드 록실기 (OH)를 아미노기로 변경하면 산성 또는 중성이 아닌 분자가 발생하며 (수소 원자 또는 메틸 CH3와 같은 유기 조합 그룹을 나타낼 수있는 NR2). 카르 복실 산 (R'COOH)에서 유래 한 카르복 아미드 (R'CONR2)가 가장 중요한 클래스입니다. 구조의 설 폰산과 유사하게, RSO2NR2 설폰 아미드가 발견된다 (RSO3H). 암모니아, 아민 또는 공유 아미드는 나트륨과 같은 반응성 금속과 결합하여 이온 성 아미드 - 스트롱 알칼리 화학 물질을 형성합니다. co-nh는 아미드 그룹 공식 또는 아미드 공식입니다.
공유 아미드
포름 아미드를 제외하고, 모든 공유 암모니아 생성 아미드는 고체입니다. 탄소가 5 개 미만인 사람들은 수용성입니다. 무기 및 유기 용매는 전기의 비전 도대체입니다. 공유 아미드의 끓는 온도, 심지어 작은 분자량을 가진 아미드의 온도는 상대적으로 높습니다.
살아있는 시스템의 단백질로서, 폴리 아미드 (폴리 아미드 (폴리머라고 불리는 큰 분자를 만들기 위해 아미드))는 풍부하지만 간단한 공유 아미드의 천연 공급원은 그렇지 않습니다. 암모니아 또는 아민은 종종 산 또는 산 할로이드에 반응 할 때 간단한 아미드를 생성하는 데 사용됩니다. 니트릴과 물은 또한 그것들을 형성하기 위해 반응 할 수 있습니다.
효소, 강산 또는 알칼리가 존재하지 않는 한, 가수 분해 (물과의 화학 반응)는 공유 아미드가 산 및 아민으로 전환되는 과정입니다. 아미드의 탈수는 니트릴을 제공 할 수있다. 그러나, 고온 및 압력에서 수소에서 수소를 첨가하면 촉매가 존재하는 경우 대부분의 카르 복실 산 아미드를 아민으로 전환 할 수있다.
강력한 환원제, 리튬 알루미늄 수 소화물은 아미드를 아민으로 변환합니다. 아미드가 산 클로라이드 또는 무수물과 반응 할 때, 2 개의 카르 보닐 (CO) 그룹은 동일한 질소 원자에 부착된다.
몇몇 주요 상업용 아미드에는 에탄 아미드 (CH3CONH2), 용매, 디메틸 포름 아미드 HCON (CH3) 2, 설파 약물 및 나일론이 포함됩니다. 그것은 단백질 합성의 부산물로 형성되고 동물의 소변에서 배설 된 결정질 분자이다. 우레아는 카르 바미드 [CO (NH2) 2]로도 알려져 있습니다. 플라스틱 생성에 사용되는 요소-포름 알데히드 수지를 합성하기 위해서는 대량의 암모니아 및 이산화탄소가 필요합니다.
아미드의 명칭
아미드가 무엇인지, 어떻게 언급되는지 살펴 보겠습니다. 표준 명명법은 마지막 음절 이전에 접미사“아미드”를 부모의 이름에 추가합니다. 아세트산은 아미드 아세트 아미드를 생성합니다. CH3Conh2는 아미드 구조의 예입니다. IUPAC (International Union of Pure and Applied Chemistry)는 에탄 아미드의 표준 용어를 권장하지만,이 공식 이름은 거의 사용되지 않습니다. 1 차 또는 2 차 아민에서 유래 한 아미드의 이름으로 질소 치환기가 먼저 나타납니다.
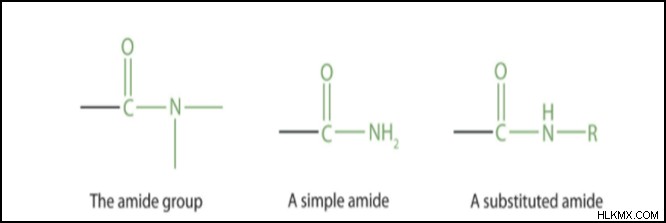
는 산 아미드 포뮬러 또는 아미드 포뮬러입니까?
입니다.디메틸 아민을 아세트산과 반응시킴으로써 생성 된 아미드 구조는 n, n- 디메틸 아세트 아미드 (CH3Conme2,) 생성된다. 전체 용어조차도 디메틸 아세트 아미드조차도 종종 약칭됩니다. 락탐은 2 차 또는 3 차로 분류 될 수있는 주기적 아미드입니다.
아미드 제조
질소 원자는 아미드의 탄소 원자에 결합되어 아미드가됩니다. 아민과 마찬가지로 아미드에는 다양한 명명 요구 사항이 있지만 모두 클래스 별 접미사-아미드가 있습니다.
카르 복실 산은 아민 또는 암모니아와 결합하여 아미드 화 과정 동안 아미드를 형성합니다. 과정에서 물 분자가 제거되면 아미드는 카르 복실 산과 아민의 나머지 부분에서 생성됩니다.
아민 및 카르 복실 산으로부터 아미드의 합성은 본질적으로 생물학적 과정이다. 아미노산의 중합 (카르 복실 산이 아민으로 대체되는 분자 사슬)의 중합을 통해 단백질이 합성된다.
아미드 범주
아미드를 탐색하기 전에 이름이든 구조이든 어휘에 대한 기본 사항을 이해해야합니다. 명칭에 따르면, 아민은 1 차 아민, 2 차 아민 및 3 차 아민의 세 가지 범주로 분류됩니다. 차이는 분자 사슬에서 탄소 원자에 대한 질소 원자의 위치에 따라 분류된다. 1 차 아미드는 각각 "IC 산"또는 "OIC 산"의 끝에 접미사 "아미드"를 추가함으로써 식별 될 수 있습니다.
."2 차 아미드"라는 용어는 질소가 알킬기에 연결되어 있음을 나타 내기 위해 n을 통합합니다. 알킬기는 수소 및 탄소 원자를 함유하는 탄화수소 사슬입니다.
기능 그룹 아미드
식별 및 인식은보다 거대한 분자에서 아미드 기능 그룹을 사용함으로써 달성됩니다. 기능 그룹의 예는 알칸, 알코올 및 아미드입니다. 카르 복실 산 활성 그룹은 카르 보닐기를 갖는 기능 그룹 및 질소 원자를 일으킬 수 있습니다.
아미드 분자 프레임 워크
아미드 구조를 이해하려면 아미드 분자가 질소 원자를 가져야한다는 것을 아는 것이 중요합니다. 카르 보닐기에서, 2 개의 탄소 원자는 산소 원자에 결합되어 2 개의 이중 결합을 형성한다. 다른 아민 그룹은 단일 질소 원자가 R 그룹과 결합하는 단일 그룹이다. R 그룹을 구조에서 치환기로 생각할 수 있습니다. 마지막으로, 단일 결합만이 아미드를 구별하는 기능 그룹 역할을합니다.
염기성
반면에아미드는 약한베이스입니다. 아민의 컨쥬 게이트 산 (약 9.5)의 PKA와는 반대로 아미드의 컨쥬 게이트 산의 약 0.5입니다. 결과적으로, 물에서, 아미드는 뚜렷한 산-염기 거동으로 나타나지 않습니다. 염기성의 부재는 카르 보닐이 아민에서 전자를 제거하기 때문입니다. 아미드의 컨쥬 게이트 산의 PKA는 6에서 10까지 다양하므로 카르 복실 산, 에스테르, 알데히드 및 케톤보다 훨씬 더 강력한 염기가 있습니다.
결론
많은 다른 기능 그룹 중에서 아미드는 질소, 수소 또는 단일 결합에 의해 연결된 카르 보닐 그룹이다. 그룹 또는 아미드 공식은 Co-n입니다.
아미드 분자는 질소 원자를 가져야합니다. 명칭에 따르면, 아민은 1 차 아민, 2 차 아민 및 3 차 아민의 세 가지 범주로 분류됩니다. 차이는 분자 사슬에서 탄소 원자에 대한 질소 원자의 위치에 따라 분류된다. 1 차 아미드는 각각 "IC 산"또는 "OIC 산"의 끝에 접미사 "아미드"를 추가함으로써 식별 될 수 있습니다.
.