주요 차이 - 탄소 12 대 탄소 14
일부 요소는 동위 원소로 알려진 다른 형태로 존재할 수 있습니다. 원소의 동위 원소는 동일한 수의 전자와 양성자를 함유하지만 다른 수의 중성자를 포함합니다. 따라서, 그것이 같은 요소를 가지고 있더라도 질량은 다릅니다. 요소의 질량 수는 핵에서 중성자와 양성자의 합입니다. 따라서 동위 원소는 질량 수로 표시됩니다. 예를 들어, 탄소는 세 가지 형태로 존재하는 요소입니다. 다시 말해, 탄소는 3 개의 동위 원소를 가지고있다 :Carbon-12, Carbon-13 및 Carbon-14. 카본 -12의 질량 수는 6 개의 중성자와 6 개의 양성자를 함유하고 있기 때문에 12입니다. 마찬가지로, 탄소 -13 동위 원소는 7 개의 중성자와 6 개의 양성자를 함유하고, Carbon-14 동위 원소에는 8 개의 중성자와 6 개의 양성자가 포함됩니다. 동위 원소를 갖는 대부분의 요소는 본질적으로 풍부하게 존재하는 하나의 주요 동위 원소를 갖는 반면, 나머지 동위 원소는 매우 작은 비율로 존재합니다. 따라서, 원소의 상대 원자 질량을 고려할 때, 일반적으로 상대 질량 수는 주요 또는 존재하는 기존 동위 원소의 질량 수와 같다고 가정한다. 탄소 12와 탄소 14 동위 원소의 주요 차이점은 안정성입니다 ; 탄소 12 동위 원소는 탄소 14보다 안정적입니다 .
주요 영역을 다루었습니다
1. 탄소 12
- 정의, 구조, 속성
2. 탄소 14
- 정의, 구조, 속성
3. Carbon 12와 Carbon 14의 차이점은 무엇입니까
- 주요 차이점 비교
주요 용어 :동위 원소, 탄소, 탄소 동위 원소, 질량 수, 중성자, 탄소 12, 탄소 14, 방사능, Avogadro Constant 
탄소 12
Carbon-12 동위 원소는 자연적으로 발생하는 모든 탄소의 약 98.89%를 구성하는 가장 풍부한 탄소 동위 원소입니다. 그것은 모든 생물학적 시스템에서 발견됩니다. Carbon-12 원자는 핵에 6 개의 중성자와 6 개의 양성자를 함유한다. Carbon-12 동위 원소는 안정적이며 방사성이 아닙니다. 따라서 Carbon-14와 달리 부패하지 않습니다. Carbon-12 원자는 상대 원자 질량 스케일을 정의하는데 사용되며, 여기서 다른 원자의 질량은 Carbon-12 동위 원소의 덩어리와 비교된다. 여기서, Carbon-12는 표준 원자로 간주됩니다. 요소의 상대 원자 질량 (RAM)은 주기율표에 표시됩니다. 램과 마찬가지로, 두더지는 Carbon-12 동위 원소를 기반으로합니다. 카본 -12의 12.00 g에서 원자의 수는 두더지를 정의하기위한 표준으로 간주된다. 카본 -12의 12g에서 정확한 원자 수는 6.02 x 10 인 것으로 밝혀졌습니다. . 이탈리아 화학자 인 Amedeo Avogadro는 19 세기 에이 수치를 발견했습니다. 이 숫자는 avogadro constant 로 정의됩니다 . Avogadro 상수의 단위는 mol.
입니다탄소 14
Carbon-14는 불안정한 탄소 동위 원소이며 8 개의 중성자와 6 개의 양성자가 포함되어 있습니다. 따라서 질량 수는 14입니다. 다른 동위 원소와는 달리, 탄소 -14는 방사능입니다. 따라서 시간이 지남에 따라 쇠퇴합니다. Carbon-14 동위 원소는 모든 자연 발생 탄소의 약 0.01% 미만을 구성합니다. Carbon-14의 붕괴 작용은 자발적이다. 탄소 -14는 질소 -14 원자를 형성하기 위해 붕괴된다. 유기체는 광합성 또는 유기물을 섭취하는 동안 탄소 -14를 얻습니다. 유기체가 죽으면 Carbon-14 공급원 복용을 중단합니다. 이를 통해 Carbon-14는 부패하기 시작하여 약 5730 년 만에 초기 금액의 절반이되며, 이는 Carbon-14의 반감기라고합니다. 나머지 양의 탄소 -14는 대부분의 살아있는 표본에 존재하는 양과 비교할 수 있으며, 측정 될 수있다. 그렇게함으로써 과학자들은 Carbon-14를 사용하여 화석의 나이를 결정할 수 있습니다. 그러나, Carbon-14는 50,000 년이 지난 후 50,000 년이 지난 후 50,000 년이 지난 화석에 적용됩니다.
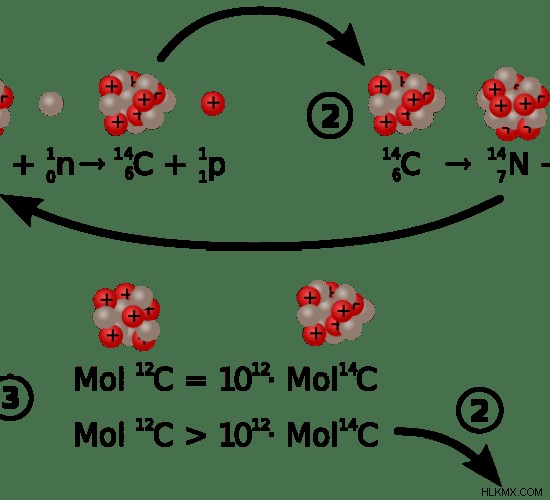
그림 1 :탄소 14의 형성 및 붕괴
탄소 12와 탄소 14의 차이
질량 수
Carbon-12 : Carbon-12의 질량 수는 12입니다.
Carbon-14 : 카본 -14의 질량 수는 14입니다.
원자에서 중성자 수
Carbon-12 : Carbon-12에는 6 개의 중성자가 있습니다.
Carbon-14 : Carbon-14에는 8 개의 중성자가 있습니다.
안정성
Carbon-12 : Carbon-12는 안정적입니다.
Carbon-14 : 카본 -14는 불안정하다.
방사능
Carbon-12 : Carbon-12는 방사성이 아닙니다.
Carbon-14 : Carbon-14는 방사성입니다.
응용
Carbon-12 : Carbon-12는 모든 생물학적 시스템의 빌딩 블록입니다.
Carbon-14 : Carbon-14는 50,000 세로 거슬러 올라가는 화석의 나이를 측정하는 데 사용됩니다.
동위 원소 분포
Carbon-12 : Carbon-12는 모든 자연 발생 탄소의 99%에서 발견됩니다.
Carbon-14 : Carbon-124는 모든 자연 발생 탄소의 0.01% 미만을 구성합니다.
결론
Carbon-12와 Carbon-14는 두 가지 유형의 동위 원소입니다. Carbon-12는 가장 풍부한 탄소 동위 원소이며 방사능이 없기 때문에 안정적입니다. 그러나, 탄소 -14는 방사능으로 인해 안정적이지 않다. 그로 인해 탄소 -14는 생물학적 시스템에서 거의 발견되지 않습니다. 이것은 Carbon-12와 Carbon-14의 차이입니다.
참조 :
1. Breithaupt, Jim. 물리학 (Palgrave Foundations Series). N.P. :Palgrave MacMillan;, 2010. print.
2. Knorr, Susan. 원자에 대해 배우고 있습니다. Greensboro, NC :Mark Twain Media, 2004. Print.
이미지 제공 :
1. C14_Methode_physikalische_grundlagen.svg :SgbeerDerivative Work :Niknaks Talk-갤러리-위키 백과-C14_Methode_Physikalische_grundlagen.svg (CC By-Sa 3.0)를 통해 wikimedia







