주요 차이 - 방사형 대 각도 노드
원자 궤도 또는 전자 궤도는 전자를 가장 높은 확률로 찾을 수있는 원자의 영역입니다. 원자는 원자의 중심에 양성자와 중성자를 함유하며, 이는 핵이라고 불린다. 핵에는 전자가 없습니다. 전자는 핵 주위에 분산됩니다. 그러나 이들 전자는 전자 궤도 또는 전자 쉘로 알려진 특정 경로에서 핵 주위에 움직이고있다. 이 전자 쉘은 서브 쉘로 구성됩니다. 각 운동량 양자 수에 따라, 서브 쉘은 하나 이상의 궤도와 같은 궤도, p 궤도, d 궤도 및 f 궤도를 포함한다. 이 궤도는 다른 평면에있을 수 있습니다. 특정 평면의 각 궤도는 로브 로 알려져 있습니다. . 전자는이 엽 내에서 발견됩니다. 그러나 전자를 찾을 수없는 비행기가 있습니다. 이것을 노드 이라고합니다 . 방사형 노드와 각도 노드와 같은 두 가지 유형의 노드가 있습니다. 방사형 노드와 각도 노드의 주요 차이점은 방사형 노드가 구형이고 각도 노드는 일반적으로 평평한 평면이라는 것입니다.
주요 영역을 다루었습니다
1. 로브와 노드는 무엇입니까
- 로브와 노드의 설명
2. 방사형 노드
- 정의, 모양 및 결정
3. 각도 노드
- 정의, 모양 및 결정
4. 방사형 및 각도 노드의 유사점은 무엇입니까
- 일반적인 기능의 개요
5. 방사형 및 각도 노드의 차이점은 무엇입니까
- 주요 차이점 비교
주요 용어 :각 노드, 원자, 원자 궤도, 전자, 전자 쉘, 로브, 노드, 핵, 방사형 노드, 양자 번호

엽 및 노드
가장 먼저, 로브가 무엇인지 제대로 이해해야합니다. 소개에서 설명한 바와 같이, 원자는 양성자, 중성자 및 전자로 구성된다. 양성자와 중성자는 원자의 중심에 있으며, 이는 핵이라고 불립니다. 그러나 핵에는 전자가 없습니다. 전자는 핵 주위에서 지속적인 움직임에 있습니다. 그들은 임의의 경로에서 움직이지 않습니다. 전자가 위치 할 수있는 특정 경로가 있습니다. 이들은 전자 껍질로 알려져 있습니다. 전자 쉘은 전자가 확률이 가장 높은 영역입니다.
전자 껍질은 핵과 다른 거리에 있습니다. 그들은 구체적이고 불연속 에너지를 가지고 있습니다. 따라서 이러한 전자 쉘은 에너지 수준이라고도합니다. 이것들은 가장 가까운 핵에서 시작하는 k, l, m, n 등으로 명명됩니다. 가장 작은 전자 쉘은 에너지가 가장 낮습니다.
각각의 모든 전자 쉘은 양자 번호를 사용하여 특징 지어집니다. 전자 쉘에는 서브 쉘이 있습니다. 이 서브 쉘은 궤도로 구성됩니다. 이 궤도는 해당 궤도에서 전자의 각 운동량에 기초하여 서로 다릅니다. 이 궤도에는 모양도 다릅니다. 서브 쉘은 s, p, d 및 f.
로 지명됩니다.서브 쉘은 다른 평면에 로브 (궤도)가 있습니다. 로브는 전자가 상주하는 영역입니다. 이 엽의 크기, 모양 및 수는 다른 궤도에 대해 서로 다릅니다.
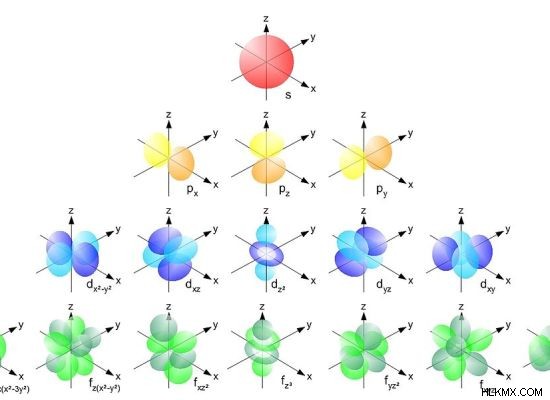
그림 1 :궤도의 다른 엽
위의 이미지에서 볼 수 있듯이 로브는 다른 평면에 있습니다. 궤도를 볼 수없는 평면을 노드라고합니다. 노드에는 전자가 없습니다. 따라서 노드는 전자가 발견 될 확률이 0 인 영역입니다. 예를 들어, 위의 이미지에 주어진대로 평면 d xz 에 대한 궤도는 없습니다. 및 d
방사형 노드
방사형 노드는 전자를 찾을 확률이 0 인 구형 영역입니다. 이 구체에는 고정 반경이 있습니다. 따라서, 방사형 노드는 방사형 적으로 결정된다. 방사형 노드는 주요 양자 수가 증가함에 따라 발생합니다. 주요 양자 수는 전자 쉘을 나타냅니다.
방사형 노드를 찾을 때 방사형 확률 밀도 함수를 사용할 수 있습니다. 방사상 확률 밀도 함수는 전자가 양성자로부터의 거리 r에 위치한 지점에있는 확률 밀도를 제공한다. 다음 방정식은이 목적으로 사용됩니다.
ψ (r, θ, φ) =r (r) y (θ, φ)
여기서 ψ는 파동 함수, r (r)는 방사형 성분 (핵으로부터의 거리에만 의존)이고 y (θ, φ)는 각 성분입니다. R (r) 구성 요소가 0이되면 방사형 노드가 발생합니다.
angular 노드
각도 노드는 전자를 찾을 확률이 0 인 평평한 평면 (또는 원뿔)입니다. 이것은 우리가 각도 (또는 다른) 노드에서 전자를 찾을 수 없다는 것을 의미합니다. 방사형 노드는 고정 반지름에 위치하지만 각도 노드는 고정 각도에 있습니다. 원자에 존재하는 각도 노드의 수는 각 운동량 양자 수에 의해 결정된다. 각도 노드는 각 운동량 양자 수가 증가함에 따라 발생합니다.
방사형 및 각도 노드 간의 유사성
- 둘 다 전자를 찾을 수없는 원자의 영역을 나타냅니다.
- 두 유형 모두 양자 수에 따라 다릅니다.
방사형 및 각도 노드 간의 차이
정의
방사형 노드 : 방사형 노드는 전자를 찾을 확률이 0 인 구형 영역입니다.
각도 노드 : 각도 노드는 전자를 찾을 확률이 0 인 평평한 평면 (또는 원뿔)입니다.
모양
방사형 노드 : 방사형 노드는 구형입니다.
각도 노드 : 각도 노드는 평면 또는 원뿔입니다.
특성 특성
방사형 노드 : 방사형 노드에는 고정 반지름이 있습니다.
각도 노드 : 각도 노드에는 고정 각도가 있습니다.
노드 수
방사형 노드 : 원자에 존재하는 방사형 노드의 수는 주요 양자 수에 의해 결정됩니다.
각도 노드 : 원자에 존재하는 각도 노드의 수는 각 운동량 양자 수에 의해 결정됩니다.
결론
노드는 전자를 찾을 수없는 원자의 영역입니다. 방사형 노드와 각도 노드와 같은 두 가지 유형의 노드가 있습니다. 방사형 노드와 각도 노드의 주요 차이점은 방사형 노드가 구형이고 각도 노드는 일반적으로 평평한 평면이라는 것입니다.