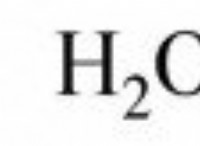Zn (S) + O2 (G) + 2H2O (L) → Zn (OH) 2 (S) + H2 (G)
이 반응에서, 아연 금속은 산화되어 아연 이온 (Zn2+)을 형성하는 반면, 산소는 수산화 이온 (OH-)을 형성하도록 감소된다. 이어서, 아연 이온은 수산화 이온과 반응하여 수산화 아연을 형성하는데, 이는 백색, 젤라틴 침전물이다. 반응에서 생성 된 수소 가스는 기포로 방출된다.
아연의 부식 속도는 환경에서 온도, 습도 및 다른 화학 물질의 존재를 포함한 여러 요인에 따라 다릅니다. 일반적으로 온도와 습도가 높을수록 부식 속도가 빨라집니다. 해수에서 발견 된 것과 같은 클로라이드 이온 (Cl-)의 존재는 또한 아연의 부식을 가속화 할 수 있습니다.
아연을 부식으로부터 보호하기 위해 종종 페인트 또는 다른 실란트의 보호 층으로 코팅됩니다. 아연은 또한 부식성을 향상시키기 위해 구리 또는 알루미늄과 같은 다른 금속과 합금 될 수 있습니다.