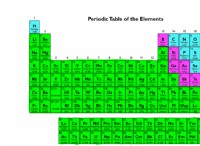
각 그룹의 이름과 특성은 다음과 같습니다.
그룹 1 : 알칼리 금속으로도 알려진이 요소는 반응성이 높고 기본 산화물을 형성합니다. 그들은 1 개의 원자가 전자를 가지고 있습니다.
예 :리튬 (Li), 나트륨 (NA), 칼륨 (k)
그룹 2 : 알칼리성 지구 금속으로 알려진이 요소는 적당히 반응성이며 기본 산화물을 형성합니다. 그들은 2 개의 원자가 전자를 가지고 있습니다.
예 :베릴륨 (BE), 마그네슘 (MG), 칼슘 (CA)
그룹 13 : 또한 triels라고도하는이 요소는 3 개의 원자가 전자를 가지며 일반적으로 +3 산화 상태에서 화합물을 형성합니다.
예 :붕소 (B), 알루미늄 (AL), 갈륨 (GA)
그룹 14 : 테트 렐이라고 불리는이 요소는 4 개의 원자가 전자를 가지며 공유 화합물을 형성하는 경향이 있습니다.
예 :탄소 (C), 실리콘 (SI), 게르마늄 (GE)
그룹 15 : PNICTOGENS로도 알려진이 요소는 5 개의 원자가 전자를 가지며 일반적으로 +5, +3, 또는 -3의 산화 상태를 나타냅니다.
예 :질소 (N), 인 (P), 비소 (AS)
그룹 16 : 칼 코겐이라고하는이 요소는 6 개의 원자가 전자를 가지며 다양한 산화 상태가있는 화합물을 형성합니다.
예 :산소 (O), 황 (S), 셀레늄 (SE)
그룹 17 : 할로겐으로 알려진이 요소들은 금속과 소금을 형성하는 반응성이 높은 비금속입니다. 그들은 7 개의 원자가 전자를 가지고 있습니다.
예 :불소 (F), 염소 (CL), 브롬 (BR)
그룹 18 : 고귀한 가스라고도하는이 요소는 매우 반응하지 않으며 완전한 외부 전자 쉘이 있습니다.
예 :헬륨 (HE), 네온 (NE), 아르곤 (AR)
이들 그룹을 이해하는 것은 주기율표에서의 위치를 기반으로 요소의 화학적 거동과 특성을 예측하는 데 필수적이다.