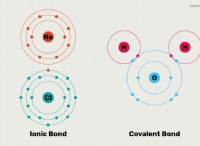
이온 성 결합은 한 원자에서 다른 원자로 전자를 완전히 전달할 때 형성되어 양으로 전하 된 이온 (양이온) 및 음이온 (음이온)이 형성됩니다. 이 반대로 하전 된 이온들 사이의 정전기 인력은 화합물을 함께 유지한다.
이온 결합의 특성 :
- 전자의 전달을 포함하여 이온의 형성으로 이어집니다.
- 이온 사이의 강한 정전기 인력.
- 화합물은 일반적으로 실온에서 결정질 고체입니다.
- 강한 이온 상호 작용으로 인한 높은 용융 및 끓는점.
- 일반적으로 극성 용매 (예 :물)에 용해되지만 비극성 용매에 불용성이 있습니다.
- 용해되거나 녹을 때 전기를 전도하여 이온의 움직임을 허용합니다.
공유 결합 :
공유 결합은 안정적인 전자 구성을 달성하기 위해 둘 이상의 원자가 전자를 공유 할 때 형성됩니다. 공유 전자는 원자 핵 사이에 국한되어 강한 결합을 형성한다.
공유 결합의 특성 :
- 원자 사이에 전자 공유가 포함됩니다.
- 공유 전자 쌍으로 인한 원자들 사이의 강한 인력.
- 화합물은 실온에서 고체, 액체 또는 가스로 존재할 수 있습니다.
- 이온 성 화합물에 비해 용융 및 끓는점이 낮습니다.
- 일반적으로 극성 용매에는 불용성이지만 비극성 용매에 용해됩니다.
- 전자가 전자가 비편화되는 금속과 같은 특수한 경우를 제외하고 전기 도체가 열악합니다.
요약하면, 이온 성과 공유 결합의 주요 차이는 전자 전달 또는 공유의 특성에있다. 이온 결합은 이온들 사이의 완전한 전자 전달 및 정전기 인력을 포함하는 반면, 공유 결합은 안정성을 달성하기 위해 원자들 사이의 전자 공유를 포함한다. 이러한 차이는 결정 구조, 용해도 및 전기 전도성과 같은 별개의 특성으로 이어집니다.