1. 에너지 생산 :
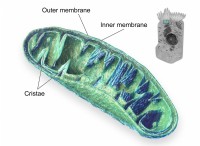
* 세포 호흡 : 산화는 우리 몸이 음식으로부터 에너지를 얻는 방법의 핵심 과정입니다. 포도당은 산화되어 세포에 연료를 공급하는 데 사용되는 에너지를 방출합니다.
* 연소 : 목재 및 휘발유와 같은 연료의 연소는 이들 물질의 빠른 산화를 포함하여 열과 빛을 방출합니다.
2. 부식 :
* 녹음 : 철에 녹의 형성은 산화의 전형적인 예입니다. 철은 물이 존재할 때 산소와 반응하여 전자를 잃고 산화철 (녹)을 형성합니다.
3. 합성 및 분해 :
* 유기 화학 : 산화는 유기 분자의 합성 및 파괴에 중요합니다. 예를 들어, 알코올은 알데히드 또는 케톤으로 산화 될 수 있습니다.
* 생화학 : 산화는 지방의 파괴 및 호르몬 생성을 포함하여 많은 대사 반응에 관여합니다.
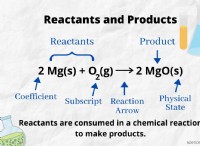
4. 화학 반응 :
* 산화 환원 반응 : 산화는 항상 물질이 전자를 얻는 과정 인 환원과 함께 발생합니다. 이러한 결합 된 반응은 산화 환원 반응으로 알려져 있으며, 이는 많은 중요한 화학 공정을 주도합니다.
5. 환경 화학 :
* 오존 형성 : 상부 대기에서 오존의 형성은 산소 분자의 산화를 포함한다.
* 대기 오염 : 대기에서 이산화황과 같은 오염 물질의 산화는 산성비에 기여합니다.
키 테이크 아웃 :
* 산화는 물질에 의한 전자 손실입니다.
* 에너지 생산, 부식, 합성 및 분해와 관련된 기본 화학 공정입니다.
* 산화는 항상 산화 환원 반응 감소와 함께 발생합니다.
* 다양한 자연 및 산업 공정에서 중요한 역할을합니다.
산화를 이해하는 것은 다양한 화학 반응과 다양한 분야에서의 영향을 이해하는 데 필수적입니다.