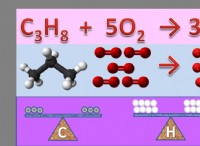
화학 방정식은 다음과 같습니다.
2 H₂ (g) + o₂ (g) → 2 h₂o (g) + 열
설명 :
* h₂ (g) 수소 가스를 나타냅니다.
* o₂ (g) 산소 가스를 나타냅니다.
* h₂o (g) 수증기를 나타냅니다.
* 열 발열 반응을 나타냅니다.
무슨 일이 일어나는지 :
* 수소 가스가 화염과 같은 점화원에 노출되면 공기 중 산소와 반응합니다.
*이 반응은 2 개의 수소 분자 (H₂)와 하나의 산소 분자 (OAT)를 결합하여 2 개의 물 분자 (HATE)를 형성합니다.
*이 과정은 상당한 양의 열과 빛을 방출합니다. 이는 수소를 태우는 불꽃으로 관찰하는 것입니다.
키 포인트 :
* 수소 연소는 매우 효율적인 반응으로 단위의 연료량 당 많은 에너지를 생성합니다.
* 깨끗한 연소 연료로 부산물로 물만 생산하여 화석 연료에 대한 유망한 대안입니다.
* 그러나 수소 가스를 취급하고 저장하려면 가연성이 높은 특성으로 인해 특별한 예방 조치가 필요합니다.