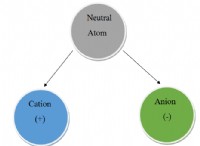
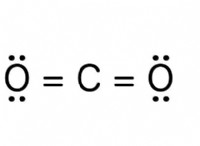* 저속 원소 (그룹 1 및 2) : 이 요소에는 하나 또는 두 개의 원자가 전자가 있습니다. 그들은 안정적인 고귀한 가스 구성을 달성하기 위해 이러한 전자를 쉽게 잃어 +1 또는 +2 충전으로 양이온을 형성합니다. 예를 들어, 나트륨 (NA)은 하나의 전자를 잃고 Na+가되고 마그네슘 (mg)은 Mg2+가되기 위해 2 개의 전자를 잃게된다.
* 높은 원자가 요소 (그룹 16 및 17) : 이 요소에는 6 ~ 7 개의 원자가 전자가 있습니다. 그들은 외부 껍질을 채우고 안정적인 고귀한 가스 구성을 달성하여 -2 또는 -1 전하로 음이온을 형성하는 전자를 얻는 경향이 있습니다. 예를 들어, 산소 (O)는 2 개의 전자를 얻어 O2-가되고 염소 (Cl)는 하나의 전자를 얻기 위해 이득을 얻는다.
원자가가 적당한 요소가 아닌 이유는 무엇입니까?
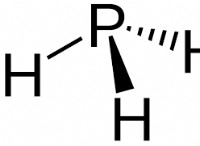
중간 정도의 원자가 (약 4)를 갖는 요소는 공유 결합을 형성하는 경향이 있으며, 전자를 공유하여 전자를 완전히 얻거나 완전히 잃지 않고 안정성을 달성합니다. 이들은 외부 껍질이 가득 차 있기 때문에 전자를 완전히 제거하거나 얻지 않고 전자를 공유하는 것이 활발하게 유리하기 때문입니다.
예외 :
이 일반적인 규칙에는 특히 여러 원자가를 가질 수있는 전이 금속에서는 예외가 있습니다. 그러나 일반적인 원칙은 안정적인 고귀한 가스 구성을 달성하기 위해 전자를 얻거나 잃는 경향이 강한 요소가 가장 쉽게 이온을 형성하는 요소라는 사실을 알 수 있습니다.