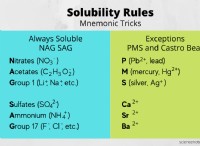
* 이온 성 화합물 : 염 (NaCl)은 이온 성 화합물입니다. 물에 용해 될 때, 그것은 나트륨 이온 (Na+) 및 클로라이드 이온 (Cl-)에 구성된 이온으로 분리됩니다. 이 이온은 용액 내에서 자유롭게 움직일 수 있습니다.
* 충전 캐리어 : 이들 유리한 하전 된 이온의 존재는 전기가 용액을 통해 흐를 수있게한다. 이온은 전기장에 반응하여 이동하는 전하 담체로서 작용한다.
* 전도도 : 염 용액의 전도도는 다음과 같은 요인에 따라 다릅니다.
* 소금 농도 : 염 농도가 높을수록 이온이 더 많아서 전도도가 향상됩니다.
* 온도 : 온도가 높을수록 이온 이동성이 증가하여 전도도가 향상됩니다.
* 소금 유형 : 염은 다른 해리 상수를 가지며 전도도에 영향을 미칩니다.
대조적으로, 순수한 물은 매우 열악한 전기 도체 입니다. 자유 이온이 거의 없기 때문입니다. 그러나 물에 소금을 첨가하면 전도도가 크게 증가합니다.