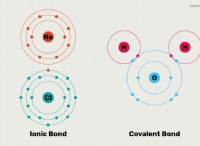
에너지 및 화학 결합
* 결합 형성 : 원자가 결합하여 분자를 형성하면 에너지가 방출됩니다. 이는 전자를 공유하거나 전달함으로써 원자가 더 안정적이되기 때문에이 안정성은 에너지 방출에 반영되기 때문입니다.
* 채권 파괴 : 기존 채권을 깨뜨려면 에너지 입력이 필요합니다. 막대기를 부러 뜨리기 위해 에너지가 필요하다고 생각하십시오.
발열 반응 :에너지가 방출됩니다
* 제품은 반응물보다 더 안정적입니다 : 형성된 생성물은 더 강한 결합을 가지며 반응물보다 더 안정적이다.
* 에너지는 열로 방출됩니다 : 더 강한 결합을 형성함으로써 여분의 에너지는 종종 열로 방출되어 주변 환경을 따뜻하게 만듭니다.
* 예 : 연소 (연소 연료), 다이너마이트 폭발, 철의 녹슬
흡열 반응 :에너지는 흡수됩니다
* 제품은 반응물보다 덜 안정적입니다 : 형성된 생성물은 결합이 약하고 반응물보다 덜 안정적이다.
* 에너지는 주변 환경에서 흡수됩니다. 주변 환경에서 가져온 기존 채권을 깨뜨리려면 에너지가 필요합니다.
* 예 : 광합성, 녹는 얼음, 질산 암모늄 용해
키 포인트
* 에너지는 보존됩니다 : 화학 반응에서의 총 에너지량은 동일하게 유지됩니다. 에너지는 단순히 전송되거나 변형됩니다.
* 엔탈피 변화 (ΔH) : 이것은 반응의 열 에너지 변화의 척도입니다. 음성 ΔH는 발열 반응을 나타내고, 양성 ΔH는 흡열 반응을 나타낸다.
* 활성화 에너지 : 발열 반응조차도 결합을 파괴하기 위해 초기 에너지의 입력이 필요합니다. 이것을 활성화 에너지라고합니다.
간단한 용어 : 집을 짓는 것과 같은 화학 반응을 생각하십시오.
* 발열 반응 : 당신은 강한 기초가있는 튼튼한 집을 짓습니다. 이 과정은 완성 된 집에서 태양의 따뜻함처럼 에너지를 방출합니다.
* 흡열 반응 : 당신은 튼튼한 집을 해체하여 벽과 기초를 분해하기 위해 에너지가 필요합니다. 이것은 철거 도구를 가열 해야하는 것과 같은 에너지가 필요합니다.