알칼리성 금속 (그룹 1)
* 낮은 이온화 에너지 : 알칼리성 금속은 가장 바깥 쪽 쉘에 전자가 하나뿐입니다. 이 전자는 비교적 쉽게 제거하므로 이온화 에너지가 낮아야합니다. 이것은 그들이이 전자를 잃고 양의 이온 (양이온)을 형성하기를 간절히 원합니다.
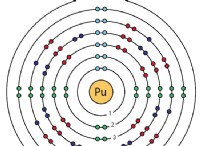
* 큰 원자 반경 : 알칼리성 금속은 가장 바깥 쪽 쉘의 단일 전자가 핵에서 멀어져서 큰 원자 반경을 가지고 있습니다. 이것은 그들의 가장 바깥 쪽 전자가 느슨하게 고정되어있어 쉽게 제거 할 수 있음을 의미합니다.
* 전기 양성 특성 : 전자를 잃고 양성 이온을 형성하는 경향은 전기 양성을 만듭니다.
할로겐 (그룹 17)
* 높은 전자 친화력 : 할로겐은 가장 바깥 쪽 껍질에 7 개의 전자가 있습니다. 안정적인 옥켓 구성을 달성하기가 부족한 하나의 전자입니다. 전자를 얻는이 강한 욕구는 그들에게 높은 전자 친화력을 제공하여 그들을 매우 반응성으로 만듭니다.
* 작은 원자 반경 : 할로겐은 알칼리성 금속에 비해 원자 반경이 작습니다. 이것은 그들의 가장 바깥 쪽 전자 쉘이 핵에 더 가깝기 때문에 추가 전자에 대한 더 강한 인력을 얻는다는 것을 의미합니다.
* 전기 음성 특성 : 전자를 얻고 음이온 (음이온)을 형성하는 경향은 전기 음성을 만듭니다.
반응성 요약 :
* 알칼리성 금속 단일 외부 전자를 쉽게 잃어 양성 이온을 형성하기 때문에 반응성이 높습니다.
* 할로겐 그들은 옥셋을 완성하기 위해 전자를 쉽게 얻고 음이온을 형성하기 때문에 매우 반응성이 높습니다.
중요한 참고 : 반응성은 알칼리성 금속과 할로겐 모두에 대해 그룹을 감소시킨다. 이는 이온화 에너지가 알칼리성 금속에 대한 감소하고 원자 크기가 증가함에 따라 전자 친화도가 할로겐에 대해 감소하기 때문이다.