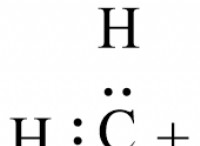1. 산화 정도 : 그것은 원자가 중립 상태에 비해 획득 또는 손실 된 전자의 수를 나타냅니다.
* 양성 산화 수 : 원자는 전자가 손실되었으므로 산화되어 있습니다.
* 음성 산화 수 : 원자는 전자를 얻었으므로 감소합니다.
* 제로 산화 번호 : 원자는 전자를 얻거나 잃어 버리지 않았습니다.
2. 결합에서의 원자의 역할 : 원자가 화학 결합에 어떻게 참여하는지 이해하는 데 도움이됩니다. 예를 들어, 양의 산화 수는 종종 원자가 양이온 (양으로 하전 된 이온)으로 작용하고 이온 성 결합을 형성한다는 것을 나타냅니다.
3. 화학 반응 예측 : 산화 수는 화학 방정식의 균형을 유지하고 산화 환원 반응의 생성물 (전자 전달과 관련된 반응)을 예측하는 데 중요합니다.
4. 화합물의 특성 결정 : 그들의 원소에 대한 산화 수가 높은 화합물은 종종 반응성이 높거나 산화제입니다.
5. 화학적 특성 이해 : 산화 수는 화합물에서 원소의 화학적 특성을 예측하는 데 사용될 수있다. 예를 들어, 산화 수가 높은 원소는 일반적으로 더 산성이며 산화 수는 낮은 요소는 더 기본적입니다.
예는 다음과 같습니다.
화합물 naCl 를 고려하십시오 (염화나트륨).
* 나트륨 (NA)의 산화 수는 +1입니다. 이것은 하나의 전자를 잃었다는 것을 의미합니다.
* 염소 (CL)의 산화 수는 -1입니다. 이것은 하나의 전자를 얻었음을 의미합니다.
이 정보는 나트륨이 산화되었고 (전자 손실) 염소가 감소했음을 알 수 있습니다 (전자 획득). 이 전자 전달은 두 요소 사이에 이온 결합을 형성하여 화합물 NaCl을 생성합니다.
전반적으로, 산화 수는 분자 내에서 원자의 행동과 상호 작용을 이해하기위한 강력한 도구이다.