왜 원소가 다수의 이온을 형성하는지
* 전이 금속 : 전이 금속은 특히 여러 이온을 형성하는 것으로 알려져 있습니다. 이것은 d 궤도에 전자가 있기 때문에 다른 방식으로 결합에 참여할 수 있기 때문입니다. 예를 들어, 철 (Fe)은 Fe²⁺ 또는 Fe³⁺로 존재할 수 있습니다.
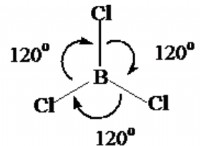
* 비금속 : 인 (P), 황 (S) 및 염소 (CL)와 같은 일부 비금속도 여러 이온을 형성 할 수 있습니다. 이것은 종종 특정 화학 환경과 그들이 얻거나 잃는 전자의 수에 달려 있습니다. 예를 들어, 황은 s²⁻, so₃²⁻ 또는 so₄²⁻ 이온을 형성 할 수 있습니다.
* 가변 산화 상태 : 상이한 이온을 형성하는 요소의 능력은 가변 산화 상태와 관련이있다. 산화 상태는 화합물에서 요소의 명백한 전하를 나타냅니다. 원소는 다수의 산화 상태를 가질 수 있고, 각 산화 상태는 다른 이온에 해당한다.
예 :
* 철 (fe) : Fe²) (철) 및 fe³⁺ (제 2)
* 구리 (Cu) : cuous (cuprous) 및 cu²⁺ (cupric)
* 크롬 (CR) : CR² ⁺ 및 Cr³ cr
* 망간 (Mn) : mn²⁺, mn³⁺, mn⁴⁺, mn⁶⁺ 및 mn⁷⁺
* 황 (s) : s²) (황화물), so₃²⁻ (황산염), so₄²⁻ (설페이트)
* 염소 (CL) : cl⁻ (염화물), 클로 ⁻ (차아 염소산염), 클로 ₂⁻ (아 염소산염), 클로에 (염소산염), Clo₄⁻ (과염소산염)
중요한 참고 : 상이한 이온의 형성은 특정 화학 반응 및 관련된 다른 요소에 의존한다. 종종이 이온이 Fe²⁺의 경우 철 (II) 및 Fe³⁺의 철 (III)과 같은 로마 숫자로 표시됩니다.