* Arrhenius acid : Arrhenius 산은 물에 용해 될 때 수소 이온 (H+)을 생성하는 물질입니다.
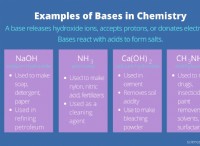
* Arrhenius Base : Arrhenius베이스는 물에 용해 될 때 수산화 이온 (OH-)을 생성하는 물질입니다.
물 자체는 자체적으로 용해 될 때 H+ 또는 OHION을 생산하지 않습니다. 그러나 그것은 autoionization 라는 과정을 겪습니다 , 그것은 산과 기저 모두 동시에 작용하는 곳 :
```
2H2O <=> H3O + + OH-
```
이 반응에서, 하나의 물 분자는 산으로서 작용하여, 다른 물 분자에 양성자 (H+)를 기부하는데, 이는 염기로서 작용한다. 이는 하이드로 늄 이온 (H3O+) 및 수산화 이온 (OH-)의 형성을 초래한다.
따라서 물은 Arrhenius 산 또는 염기의 엄격한 정의에 맞지 않지만 수륙 양용 거동을 나타내므로 다른 상황에서 산과 염기로 작용할 수 있습니다. .
이 수륙 양용의 물의 특성은 용매로서의 역할과 많은 화학 반응에 중요합니다.