Avogadro의 법칙
Avogadro의 법칙은 동일한 온도와 압력에서 동일한 부피의 가스가 동일한 수의 분자를 포함한다고 말합니다. 이것은 다음을 의미합니다.
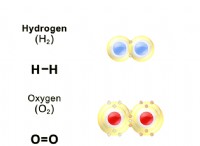
* 두더지 비율 : 균형 잡힌 화학 방정식의 계수는 반응물 및 생성물의 두더지 비율을 나타냅니다. 예를 들어, 반응 2H₂ + OAT → 2H₂O에서, 수소 대 산소의 두더지 비율은 2 :1이다.
* 볼륨 비율 : 분자의 수는 부피 (상수 t 및 p에서)에 직접 비례하기 때문에, 두더지 비율은 또한 기체 반응물 및 생성물의 부피 비율을 나타낸다. 같은 예에서, 수소 대 산소의 부피 비율은 또한 2 :1이다.
중요한 점
* 이상적인 가스 행동 : Avogadro의 법칙은 분자간 힘이 무시할 수있는 이상적인 가스에 가장 적합합니다.
* 온도와 압력 : 부피 비율은 반응 내내 온도와 압력이 일정하게 유지되는 경우에만 적용됩니다.
* 화학량 측정법 : 균형 방정식의 두더지 비율은 반응에 관여하는 반응물 및 생성물의 양을 계산하는 데 중요합니다.
예
다음과 같은 반응이 있다고 가정 해 봅시다.
n ₂ (g) + 3H₂ (g) → 2NH₃ (g)
* 두더지 비율 : 질소 대 수소 대 암모니아의 두더지 비율은 1 :3 :2입니다.
* 볼륨 비율 : 반응이 일정한 온도 및 압력에서 발생하는 경우, 질소 대 수소 대 암모니아의 부피 비율도 1 :3 :2가됩니다.
결론
균형 잡힌 화학 방정식의 두더지 비율은 Avogadro의 법칙 덕분에 일정한 온도 및 압력에서 기체 반응물 및 제품의 부피 비율로 직접 변환됩니다. 이 원칙은 화학 반응과 관련된 가스의 양을 이해하고 예측하는 데 필수적입니다.