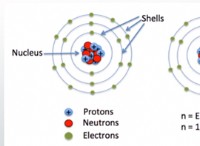
그는 전자가 원자 전체에 무작위로 분포되었거나 어디에서나 발견 될 수 있다고 제안하지 않았다. 그는 전자가 이러한 특정 에너지 수준으로 제한되어 있다고 믿었으며 불연속 패킷에서 에너지를 흡수하거나 방출함으로써 이들 사이에서만 전환 할 수 있다고 믿었다.
더 자세한 설명은 다음과 같습니다.
* bohr 모델 : Bohr의 원자 모델은 전자가 특정한 양자화 된 에너지 수준으로 핵을 공전 할 것을 제안하는 상당한 발전이었습니다.
* 에너지 수준 : 이 레벨은 사다리의 렁과 같으며 각 레벨은 다른 에너지 값을 나타냅니다. 전자는 이러한 특정 수준에서만 존재할 수 있습니다.
* 전자 및 에너지 : 전자는 에너지를 흡수하거나 방출하여 에너지 수준 사이를 이동할 수 있습니다. 이것은 에너지 수준의 "사다리"를 위 또는 아래로 이동하는 전자와 유사합니다.
Bohr의 모델은 원자 구조를 이해하는 데 귀중한 단계 였지만 시간이 지남에 따라 개선되었습니다. 현대 양자 역학은 원자의보다 정교한 그림을 제공하며, 여기서 전자는 잘 정의 된 궤도가 아닌 확률 분포 (궤도)에 의해 설명됩니다.