이산화탄소의 실험실 준비
실험실에서 이산화탄소를 준비하는 방법은 다음과 같습니다.
재료 :
* 탄산 칼슘 (CACO3) : 이것은 대리석 칩이나 석회암의 형태 일 수 있습니다.
* 희석 염산 (HCl) : 약 2m 농도.
* 전달 튜브 : 가스 흐름을 지시하는 데 사용되는 유리 튜브.
* 원뿔 플라스크 또는 비이커 : 반응 혼합물을 유지합니다.
* 공압 트로프 : 물 위에 가스를 모으기 위해.
* 가스 항아리 : 수집 된 가스를 저장합니다.
절차 :
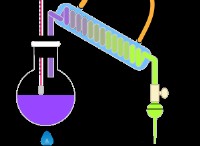
1. 장치를 설정하십시오 :
* 소량의 탄산 칼슘 (대리석 칩 또는 석회암)을 원뿔 플라스크에 넣습니다.
* 플라스크에 희석 된 염산을 첨가하십시오.
* 전달 튜브를 플라스크에 연결하여 튜브가 산 표면 바로 아래에 도달하도록합니다.
* 공압 트로프를 물로 채우고 물로 채워진 가스 병을 트로프로 뒤집습니다.
2. 이산화탄소를 수집하십시오 :
* 산이 탄산 칼슘과 접촉하면 반응이 발생합니다.
*이 반응은 이산화탄소 가스를 생산하여 전달 튜브를 통해 거품을 일으켜 가스 항아리의 물을 대체합니다.
* 가스 항아리는 이산화탄소로 채워지며 항아리가 가득 차있을 때까지 계속 수집 할 수 있습니다.
3. 가스 식별 :
* 이산화탄소를 수집했는지 확인하려면 Limewater (수산화 칼슘 용액)로 가스를 테스트하십시오.
* 가스가 이산화탄소 인 경우 탄산 칼슘의 형성으로 인해 석회질이 밀키를 돌릴 것입니다.
반응 :
이산화탄소 제조에 관여하는 화학 반응은 다음과 같습니다.
CACO3 (S) + 2HCL (AQ) → CACL2 (AQ) + H2O (L) + CO2 (g)
안전 예방 조치 :
* 적절한 안전 고글과 장갑을 착용하십시오.
* 잘 통풍이 잘되는 지역에서 일하십시오.
* 부식성이므로 염산을 취급 할 때주의하십시오.
* 산과 폐기물을 올바르게 폐기하십시오.
추가 메모 :
* 중탄산 나트륨 (베이킹 소다)을 가열하거나 목재 또는 숯과 같은 탄소를 함유 한 물질을 태워 이산화탄소를 준비 할 수도 있습니다.
* 가스는 가스 항아리 또는 기타 적합한 용기에 보관할 수 있습니다.
* 이산화탄소는 공기 가스보다 무색, 무취이며 무겁습니다.
* 일반적인 온실 가스이며 탄소 사이클에서 중요한 역할을합니다.
이 절차는 실험실 환경에서 이산화탄소를 준비하는 간단하고 효과적인 방법을 제공합니다. 그것은 준비와 관련된 화학 반응을 보여주고 간단한 화학적 테스트를 통해 수집 된 가스의 식별을 허용합니다.