* 산 물에 용해 될 때 수소 이온 (H+)을 기증하는 물질입니다.
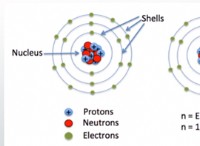
* 유리 수소 입자 반응성이 높고 일반적으로 용액에서는 발견되지 않는 개별 수소 원자를 지칭 할 수 있습니다.
* 수소 이온 (H+) 수소 원자가 전자를 잃을 때 형성됩니다. 이 이온은 산에 특징적인 특성을 제공하는 것입니다.
* 신맛
* 염기와 반응하여 소금과 물을 형성하는 능력
* 지표의 색상을 변경하는 능력 (리트머스 종이와 같은)
여기 간단한 비유가 있습니다 : 레몬을 상상해보십시오. 레몬은 산성이므로 구연산을 함유하여 수중 이온을 방출합니다. 이 수소 이온은 레몬을 먹을 때 신맛을 맛볼 이유입니다. 유리 수소 입자 자체는 신맛의 이유가 아닙니다. 책임이있는 것은 수소 이온입니다.
요약하면, 유리 수소 입자는 산의 특성과 직접 관련이 없습니다. 산도 및 관련 특성을 정의하는 것은 용액에서 수소 이온 (H+)의 존재입니다.