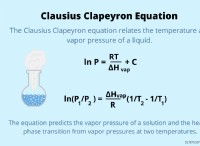
플루오로 안티 몬 산은 세계에서 가장 강한 산으로, 카보 레인 위의 약간의 받침대에 자랑스럽게 서 있습니다. 그러나 Carborane이 그들 중 가장 강한 지에 대한 논쟁은 여전히 진행 중입니다. 이 산은 너무 강해서 기존의 산으로 간주되지 않습니다. 그것들은 초고시로 표시되어 있습니다.
산과 염기의 개념은 나의 의식의 표면에 청소년의 추억의 급증을 가져옵니다. 나는 실험실 코트, 리트머스 종이, 이상한 모양의 선박에서 상승하는 매운 연기와 내 가난한 등급을 생각합니다.
실험실 코트는 단지 모든 범죄 조사 쇼에서 Guy가 착용하는 멋진 고정 관념 법의학이 입는 것이기 때문에 권장되는 것이 아닙니다. 보호 아이 기어와 함께 코트는 산, 염기, 소금 또는 기타 잠재적으로 유해한 화학 물질의 유해한 유출로부터 우리를 보호하기 때문에 권장됩니다.
옷을 뚫고 피부를 태울 수있는 산을 고려하십시오. 면 코트는 그것을 흡수하여 우리의 육체를 보호하기 위해 용감하게 희생하고 더 중요한 것은 내가 가장 좋아하는 Calvin Klein 셔츠입니다.

그러나 나는 샐러드에 식초를 조심스럽게 첨가하면서 실험실 코트와 보호 고글을 착용 한 엄마의 터무니없는 시각을 아직 목격하지 않았습니다. 얼마나 나쁜가요! 그녀는 신경 쓰지 않거나 무책임합니까? 글쎄… 아니요. 그녀는 과학적으로, 경험적으로도 식초가 강하지 않다는 것을 알고 희망적으로 알고 있습니다. 산.
산을 강하게 만드는 것은 무엇입니까? 이 경우 산을“산”으로 만드는 이유는 무엇입니까?
강산이란 무엇입니까?
산은 수소 이온 (H+)을 생성하기 위해 용액과 반응하는 이온 성 화합물이다. 산을 묘사하는보다 간결한 방법은 양성자를 쉽게 기증하는 개체입니다. 전자가없는 원자 인 이온화 된 수소 원자는 단지 양성자 일뿐입니다. 스펙트럼의 반대편에는베이스는 쉽게 받아들이는 개체입니다. 이 양성자.
Pass the Carcel의 참가자와 평행을 그릴 수 있습니다.

(사진 크레디트 :가치 수업 게임)
산이 참가자 인 경우, 약한 산은 주저하는 참가자이며, 소포를 통과하거나 양성자를 기증 할 때 비효율적입니다. 반면에 강한 산은 항상 발가락에 있고 양성자를 기증 할 때 매우 효율적입니다.
따라서 용액에서 H+ 이온의 농도가 클수록 산이 더 산성입니다.
산도 측정 객관적으로
실제로, 이것은 pH 척도의 도움으로 산도가 객관적으로 측정되는 방식입니다. 스케일은 1-14에 이르며, 여기서 1은 매우 강한 산, 7 중성 용액 및 14 매우 강한베이스를 나타냅니다.
pH 척도는 로그 척도입니다. 그것은 H+ 이온 농도 (pH의 H)의 부정적인 로그 (p로 표시)를 취합니다. 어떻게 든, 수소 이온의 농도가 감소한다면, 기본이 올라갈 때 pH가 증가 할 것입니다.

(사진 크레디트 :Flickr)
그러나 그것은 단순히 농도 일뿐 만 아니라 활동 입니다. 이 이온의. 이들 이온의 효과는 많은 요인에 의존하며 농도는 그중 하나 일뿐입니다. 단순성을 위해 집중의 개념을 계속합시다.
산을 물 용액에 용해시킴으로써 산도 척도를 얻을 수 있습니다. H+ 양이온은 자유롭게 로밍을 찾을 수 없습니다. 이들은 수 분자 (H2O)와 반응하여 하이드로 늄 이온 (H3O+) 및 수산화 이온 (OH-)을 생성합니다.
.따라서, 물에서 더 높은 농도의 H3O+ 이온은 강산의 존재를 신호한다. 양성자 또는 H+ 이온을 박탈당한 잔류 이온은 염기입니다. 따라서, 어떤 의미에서, 산과 염기는 자연적으로 쌍으로 존재한다. 물과 산 사이의 반응의 일반적인 표현은이 표현으로 설명 할 수 있습니다.
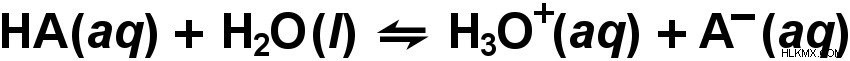
용액의 상대적 산도를 찾는 또 다른 방법 ‘ka’로 표시
위의 방정식을 언급하면
가있는 ka의 크기를 찾을 수 있습니다.
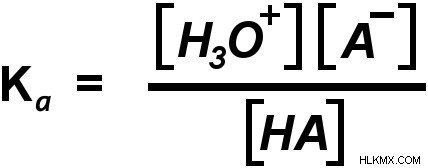
[H3O+] 및 [a-]는 리터당 두더지의 하이드로 늄 이온의 농도 및 분리 된 염기를 나타낸다. [ha]는 암묵적이고 H+ 이온을 기여하지 않은 분자의 농도입니다.
강산의 경우, 분자의 생성물은 하의 양에 비해 더 큰 값을 가지며, 분모에서 강한 산이 분할을 빠르게 촉매하고 더 많은 이온을 생성하여 HA 분자를 더 적게 남겨두기 때문에. 결과적으로 강산에 대한 KA의 값은 1보다 클 것입니다.
그러나 프로이트가 제안한 것처럼 그것은 약산입니다.
반대로, 약산의 경우, 분자의 생성물은 분모에 비해 낮은 값을 갖습니다. 왜냐하면 H+ 이온을 생산하는 데 매우 무능하기 때문입니다. 결과적으로, 약산에 대한 KA의 값은 1보다 낮을 것이다.
이런 식으로 KA의 가치는 산의 강도를 절대적인 방식으로 결정합니다.
일반적인 강산은 무엇입니까?
히드로 클로르 산 (HCl → H + + Cl-)
염산은 무색, 투명, 부식성 및 매우 강한 미네랄 산입니다. 그것은 종종 "무리아기"산이라고 불리며 벽돌이나 콘크리트를 청소하는 데 사용되는 것에 익숙 할 수 있습니다.
수소 및 염소로 형성된 이온 성 화합물 인 염산은 농도에 따라 -1에서 1 사이의 흔들림에 따라 pH 수준의 매우 강한 산입니다. 물에 거의 완전히 분리되어 Ka의 값이 매우 큽니다. 약 1.3 × 10^6.
.염산은 또한 우수한 산화제라는 명성을 얻었습니다.

(사진 크레디트 :Flickr)
그 힘에도 불구하고 놀랍게도 HCl은 대부분의 위 (위) 산을 구성합니다! 그것은 우리를 미생물, 감염으로부터 보호하며 소화에 매우 중요합니다. 점액 층은 산 자체로부터 위를 보호합니다. 점액의 분비에 실패하면 궤양이나 가슴 앓이가 발생합니다.
HCL은 부식성이 높으며 접촉 할 때 조직을 비유 적으로 태울 수 있습니다. 폐, 눈 및 피부를 돌이킬 수 없게 손상시킬 수 있습니다. 이런 이유로 항상 라텍스 장갑과 보호 화학 저항 의류로 처리해야합니다.
질산 (HNO3 → H + + NO3-)
질산은 무색, 고 부식성 미네랄 산입니다. 질산은 질화에 눈에 띄게 사용됩니다 - 질산염 그룹을 분자, 전형적으로 유기 화합물에 첨가합니다. HCL과 마찬가지로, PH 값은 -1에 가깝고 물 용액에 거의 완전히 분리되어 KA의 값도 2.4 × 10.
.

질산 연기 (사진 크레디트 :W. Oelen / Wikimedia Commons)
매우 우수한 산화제이기 때문에 비금속 및 유기물과 폭발적으로 반응합니다. 질산으로 유기 화합물의 질화는 트리 니트로 톨루엔 (TNT)과 같은 폭발물을 생성하는 두드러진 방법이다. 또한 실리콘 웨이퍼를 청소하거나 스테인레스 스틸에서 불순물을 제거하는 데에도 사용됩니다.
안전성을 위해 질산은 거만 함으로 인해 염기와 유기물로부터 멀리 떨어져있는 것이 좋습니다. 피부의 유출은 심한 화학 화상을 유발하고 즉시 살과 조직을 분해 할 수 있습니다. 구제책으로서, 많은 양의 물을 화상 부위로 투여 하여이 산을“중화”할 수 있습니다.
황산 (H2SO4 → 2H + + SO4^-2)
또 다른 고등학교가 가장 좋아하는 황산은 물과 반응하는 무색, 기름진, 강하고 부식성 미네랄 산입니다. 그것은 나무 나 유기물을 노래하는 것으로 알려져 있지만 화재를 일으키지 않을 것 같지 않습니다.

농축 황산 (황산) 방울이 면화 타월 조각을 빠르게 탈수합니다. (사진 신용 :독성 워커 / 위키 미디어 커먼즈)
사촌과 마찬가지로 황산은 약 1의 pH 를가집니다. KA 값은 1.0 × 10^3입니다. 황산은 너무 위험하여 가수 분해를 통해 일차 화상을 유발할뿐만 아니라 탈수를 통한 2 차 화상도 유발합니다. 눈에 닿는 경우 실명으로 이어질 수 있습니다.
역사적으로 황산은“vitriol의 오일”이라는 이름으로 확인되었습니다.
Fluoroantimonic Acid 병을 손에 들고 (사진 크레딧 :Game Freak / YouTube)
플루오로 안티 몬 산은 마인드 화가 pH가 -31.3입니다. 위산보다 유력한 것은 10 억억 배입니다! Looney Tunes의 Taz와 같이 컨테이너를 통해 점차 먹을 것이기 때문에 병에 보관할 수 없습니다.
그 힘의 측정은 손과 접촉 할 때 주저없이 살과 뼈를 녹일 수 있도록하는 것입니다. 그것은 테플론으로 만든 물통에 저장됩니다. 모든 유기 화학에서 가장 강력한 단일 결합이되는 것은 특전이 있습니다. 테플론은 과당에 면역됩니다.
Teflon은 또한 우리가 더 효과적으로 닭고기를 짜낼 수 있지만, 대부분, 우리는 혼란스럽고 육체와 뼈를 불완전하는 슈퍼 레이스로부터 우리를 보호하기 때문에 그것을 좋아합니다.
.