주요 차이 - 삼투압 대 강장도
삼투압과 강도라는 용어는 서로 밀접하게 관련되어 있습니다. 그들은 용액 농도의 개념과 삼투압에 어떤 영향을 미치는지를 나타냅니다. 그러나 그들이 효과를 표현하는 방식은 서로 다릅니다. 두 용어는 삼투가 발생하는 투과성 막에 의해 솔루션이 분리되는 상황과 관련이 있습니다. 삼투압은 집단 효과에 대한 용액에 존재하는 모든 분자를 고려합니다 반면, 는 용액 내에서 투과 할 수없는 용질 분자의 농도 만 고려합니다. 따라서 강모는 외부 환경의 척도라고 말할 수 있습니다 , 삼투압은 주어진 솔루션 자체에 관한 것입니다 . 이것이 주요 차이 입니다 삼투압과 강모 사이.
삼투압이란 무엇입니까
삼투압은 용액에 존재하는 삼투의 수를 '몰이성'이라고하는 용액의 두더지 수를 고려하는 잘 알려진 방법보다는 솔루션의 수를 통해 용액의 농도를 표현하는 방법입니다. 따라서 Molarity의 경우와 마찬가지로 Mol/L 대신, 삼투압은 리터당 용질의 OsMoles 또는 Osmol/L을 사용합니다. 대부분의 경우, 삼투압에 대한 값은 몰토리성의 값과 유사하지만, 수용성 화합물의 경우 삼투압은 용액의 몰보다 커집니다. 이는 삼투압이 존재하는 총 용질량을 포함하는 반면, 몰로는 전체적으로 화합물의 농도를 포함하기 때문이다. 예를 들어; NaCl은 한 번 물에 용해 된 물에 용해된다. NaCl이 처음에 2 mol/L의 농도를 가졌다면, 물의 용해시, 몰토리성은 2 mol/L로 남아 있지만, 분리 된 이온 인 용액의 총 용질 수의 고려로 인해 삼투압이 4 개의 Osmol/L로 증가합니다. (2의 Osmol/L의 Na 및 Cl의 2 Osmol/L).
주변 환경의 특성에 따라 주어진 솔루션의 삼투압은 세 가지 다른 형태를 취할 수 있습니다. 등재식, 고생물 및 저 산성. 주어진 용액의 삼투압이 주변과 동일하면 isosmotic 라고합니다. 해결책. 용액은 hyperosmotic 입니다 삼투압이 주변보다 높으면. 마찬가지로, 용액을 hypoosmotic 이라고합니다 삼투압이 주변 환경보다 낮 으면
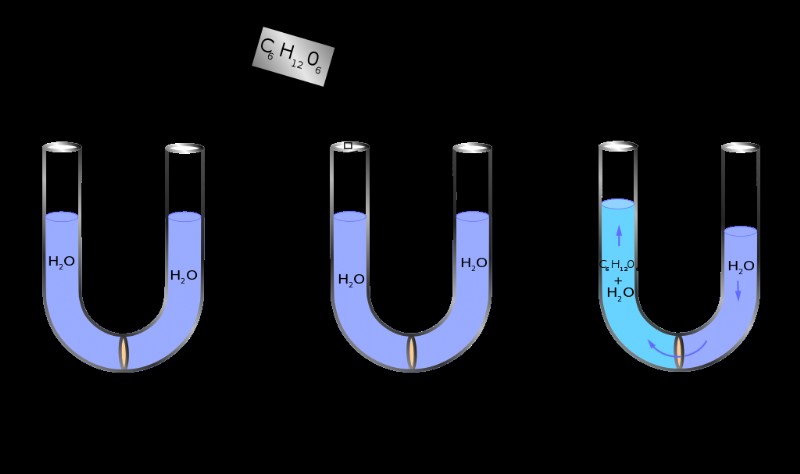
강모는 무엇입니까
삼투압과 달리 강모는 막을 통과하지 않는 용질의 영향을받습니다. 따라서 삼투압 자체가 아니라 삼투압 구배의 척도입니다. 강도의 개념은 상이한 강도의 농도에 침지 된 세포의 반응과 행동을 설명하는 데 도움이된다. 세포가 등장 용액에 배치되는 경우, 용액의 농도는 세포 함량의 농도와 유사하다. 따라서, 반 투과성 막을 통해 용매 분자의 유입 또는 유출은 없을 것이다. 그러나, 세포가 고조 론의 용액에 배치되는 경우, 용액의 농도는 세포 함량의 농도보다 높다. 따라서 용매 분자 (이 경우 물)는 농도가 막의 양쪽에서 동일 할 때까지 세포 밖으로 흐르면서 수축시킬 수 있습니다. 마찬가지로, 세포가 저혈압 용액에 배치 된 경우, 용액의 농도가 세포 내용물의 농도보다 낮으므로 세포로 물이 유입되어 세포가 팽창하고 파열되게됩니다.
.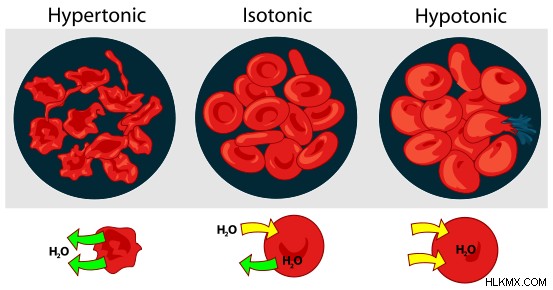
혈액 세포에 대한 다른 용액의 효과
삼투압과 강모의 차이
정의
삼투압 주어진 용액의 삼투압의 척도입니다.
강모 투과성 막으로 분리 된 두 용액 사이의 삼투압 구배의 척도입니다.
측정 단위
삼투압 Osmol/L에서 측정됩니다.
강모 농도 측정과 관련이 있으며 mol/l로 표현됩니다.
농도 정의
osmolarity 막을 관통하고 침투하지 않는 총 용질의 총 수를 고려합니다.
강모 비 투과성 용질과 관련된 농도를 고려합니다.
주변의 효과
삼투압 종종 주어진 솔루션의 분석을 나타냅니다.
강모 외부 환경의 척도로 사용됩니다.