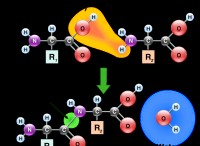
1. 산을 추가하십시오 : 가장 직접적인 방법은 용액에 산을 추가하는 것입니다. 산은 수산화물 이온 (OH-)과 조합하여 물 분자를 형성하여 오하이온의 농도를 낮추어 pH를 감소시킬 수있는 양성자 (H+)를 기증한다. 이 목적으로 사용될 수있는 일반적인 산에는 염산 (HCl), 황산 (H2SO4) 또는 질산 (HNO3)이 포함됩니다. 필요한 산의 양은 원하는 pH 및 용액의 부피에 의존 할 것이다.
2. 산성 화합물과 반응 : 또 다른 옵션은 물에 용해 될 때 산성 반응을 겪는 화합물을 도입하는 것입니다. 예를 들어, 이산화탄소 (CO2)는 물에 용해되어 탄산 산 (H2CO3)을 형성하여 H+ 이온을 방출 할 수 있습니다. 이것은 용액을 통한 CO2 가스를 버블 링하거나 드라이 아이스 또는 중탄산 나트륨 (NAHCO3)과 같은 CO2의 고체 또는 액체 공급원을 첨가함으로써 달성 될 수있다.
3. 이온 교환 : 이온 교환 수지는 용액으로부터 수산화물 이온을 제거하기 위해 사용될 수있다. 이 수지는 전형적으로 오하이온과 교환 할 수있는 음으로 하전 된 기능 그룹을 포함하는 재료로 구성됩니다. 수지는 옴을 끌어 들이고 붙잡고 pH를 효과적으로 낮추게됩니다.
4. 역 삼투 : 역삼 투는 반투과성 막을 사용하여 물에서 이온 및 기타 불순물을 제거하는 여과 과정입니다. 압력을 가해함으로써, 물은 막을 통해 강제되는 반면, 용해 된 이온의 대부분은 다른쪽에 유지된다. 이는 높은 pH가 수산화물 또는 탄산염 이온과 같은 특정 이온의 존재에 의해 야기되는 경우 용액의 pH를 낮추는 데 유용 할 수있다.
고도로 알칼리성 솔루션 (12.5의 pH)으로 작업 할 때는 안전 예방 조치를 취해야한다는 점에 유의해야합니다. 장갑, 눈 보호 및 실험실 코트와 같은 적절한 보호 장비를 항상 착용하십시오. 또한, pH를 낮추기 위해 선택된 정확한 방법은 다양한 산 또는 화합물과의 용액의 호환성, 원하는 pH 변화 속도 및 잠재적 부작용 또는 상호 작용과 같은 요인을 고려하여 특정 컨텍스트를 기반으로해야한다.