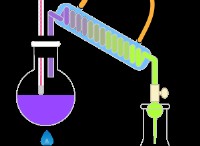
1. 에너지 흡수 : 알칼리 금속 또는 소금을 불꽃으로 가열하면 금속 원자의 전자는 열에서 에너지를 흡수합니다.
2. 여기 상태 : 이것은 에너지를 흡수하면 전자가 흥분하여 더 높은 에너지 수준으로 점프합니다. 이 흥분된 상태는 불안정합니다.
3. 빛의 방출 : 지상 상태로 돌아 가기 위해, 흥분된 전자는 빛의 형태로 흡수 된 에너지를 방출한다. 여기 상태와 접지 상태 사이의 에너지 차이는 방출 된 빛의 특정 파장 (및 색상)을 결정합니다.
왜 알칼리 금속?
알칼리 금속은 가장 바깥 쪽 껍질에 전자가 하나 뿐이며, 이는 상대적으로 느슨하게 결합된다. 이것은 전자가 에너지를 흡수하고 흥분하기가 더 쉬워집니다.
각 알칼리 금속에 대한 독특한 색상 :
각각의 알칼리 금속은 뚜렷한 에너지 수준 구조를 가지므로 지상과 여기 상태 사이의 특정 에너지 차이를 초래합니다. 에너지 수준의 이러한 차이는 독특한 파장에서 빛의 방출로 이어져 각 알칼리 금속은 특징적인 색상을 제공합니다.
* 리튬 : 크림슨 레드
* 나트륨 : 강렬한 노란색
* 칼륨 : 제비꽃
* Rubidium : 빨간색
* 세슘 : 파란색
알칼리 금속의 소금 :
알칼리 금속의 염은 알칼리 금속 양이온을 함유하기 때문에 이러한 특징적인 색상을 생성합니다. 소금이 가열되면 양이온은 에너지를 흡수하고 흥분하여 특정 파장에서 빛의 방출로 이어집니다.
요약하면, 알칼리 금속 및 소금에 대한 불꽃 테스트에서 관찰 된 특징적인 색상은 에너지를 흡수하고, 특정 파장의 빛으로 그 에너지를 방출 한 다음 금속 원자의 전자의 결과입니다.