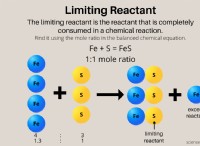
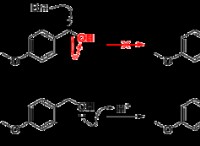
균형 화학 방정식은 다음과 같습니다.
k₄cro₂ (aq) + sr (no₃) ₂ (aq) → srcro₄ (s) + 2kno₃ (aq)
설명 :
* 칼륨 크로메이트 (k₂cro₄) 및 스트론튬 질산염 (sr (no₃) ₂) 모두 가용성 이온 성 화합물이며, 이는 물에 용해되어 이온으로 존재합니다.
* 이러한 용액이 혼합 될 때, 칼륨 크로메이트로부터의 칼륨 (k⁺) 및 크로메이트 (크로 메이트) 이온은 스트론튬 질산염으로부터 스트론튬 (SRR² ⁺) 및 질산염 (NOI) 이온과 반응한다.
*이 반응의 생성물은 Strontium Chromate (srcro₄) 입니다. 및 질산 칼륨 (Kno₃) .
* Strontium Chromate는 불용성 입니다 물에서는 용액에서 고체로 침전 될 것입니다.
반면에 질산 칼륨은 물에 용해됩니다.
관찰 :
* 당신은 노란색 침전물의 형성을 관찰 할 것입니다 용액이 혼합 될 때 (Strontium Chromate).
* 칼륨 크로메이트가 노란색이고 스트론튬 크로메이트는 더 깊고 강렬한 노란색이기 때문에 용액은 색이 변할 수 있습니다.
순 이온 방정식 :
순 이온 방정식은 침전 반응에 직접 관여하는 이온에 중점을 둡니다.
sr²r (aq) + cro₄²⁻ (aq) → srcro₄ (s)