주요 차이 - 포화 대 불포화 화합물
유기 화학에서 화학 화합물은 탄소 원자들 사이의 화학적 결합 유형에 따라 포화 또는 불포화 될 수 있습니다. 이 용어는 Alkanes, Alkenes 및 Alkynes를 설명하는 것입니다. 포화 화합물은 탄소-탄소 단일 결합으로 만 구성됩니다. 예를 들어, 알칸은 C-C 단일 결합으로 구성됩니다. 불포화 화합물은 이중 결합 및 삼중 결합을 가질 수 있습니다. 예를 들어, 알켄은 이중 결합을 포함하고 알킨은 트리플 결합을 포함합니다. 따라서 포화 화합물과 불포화 화합물의 주요 차이점은 포화 화합물은 탄소-탄소 단일 결합 만 있고 불포화 화합물은 탄소-탄소 이중 결합 및 삼중 결합을 갖는다는 것입니다. .
주요 영역을 다루었습니다
1. 포화 화합물이란 무엇입니까
- 정의, 예제에 대한 설명
2. 불포화 화합물이란 무엇입니까
- 정의, 예제에 대한 설명
3. 포화 화합물과 불포화 화합물의 차이점은 무엇입니까
- 주요 차이점 비교
주요 용어 :Alkane, Alkene, Alkyne, 방향족, 지방산, 혼성화, 포화 화합물, 불포화 화합물

포화 화합물이란 무엇입니까
포화 화합물은 탄소-탄소 단일 결합 만있는 유기 화합물입니다. 지방족 알칸과 사이클로 알칸은 포화 화합물입니다. 이 화합물은 직선 체인 일 수 있고, 측면 그룹을 가질 수 있으며, 분지 구조 또는 순환 구조 일 수 있지만 이중 결합 또는 삼중 결합이 없다.
.포화 화합물은 불포화 화합물보다 매우 반응하지 않고 더 안정적입니다. 이들 화합물은 몰 질량에 비해 낮은 용융점과 끓는점을 갖는다. C-C 결합의 모든 탄소 원자는 포화 화합물에서 SP 하이브리드 화 된 원자이다. 가장 간단한 알칸은 메탄입니다. 그것은 4 개의 탄소 원자에 결합 된 하나의 탄소 원자를 갖는다. 원자 사이에는 이중 결합 또는 삼중 결합이 없습니다. 가장 간단한 사이클로 알칸은 사이클로 프로판입니다. 3 개의 탄소 원자가 서로 결합되어 고리 구조를 형성합니다. 각각의 탄소 원자는 2 개의 수소 원자에 결합되었다; 따라서이 구조에는 이중 채권이나 트리플 본드도 없습니다.
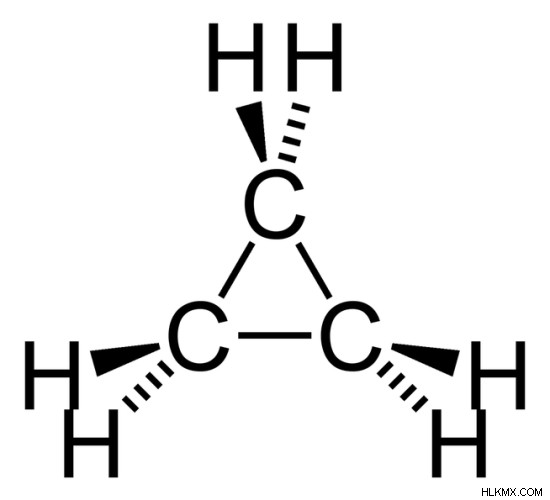
그림 1 :화학 구조는 사이클로 프로판 입니다
포화 화합물에서, 더 많은 수소 원자는 동일한 수의 탄소 원자를 갖는 불포화 화합물과 비교할 때 탄소 원자에 결합됩니다. 알칸 외에도 C-C 결합 만있는 부탄올과 1 개의 C-OH 결합이있는 알코올이있을 수 있습니다. 그러나 불포화는 없습니다. 포화 지방산은 또한 불포화 지방산과 비교할 때 포화 화합물로 간주됩니다. 포화 지방산에는 이중 결합 또는 삼중 결합이없는 포화 지방산 사슬이 있습니다.
불포화 화합물이란?
불포화 화합물은 하나 이상의 이중 결합 또는 탄소 원자들 사이의 트리플 결합을 함유하는 유기 화합물입니다. 이러한 결합은 활용 될 수 있거나 없을 수 있습니다. 공액은 다른 사람과 가역적으로 결합 된 화합물에서 화학적 결합의 존재를 지칭한다. 주요 불포화 화합물은 알켄, 알킨 및 방향족 화합물입니다.
alkenes는 하나 이상의 이중 결합을 가진 유기 화합물입니다. 이중 결합은 시그마 본드와 PI 결합으로 구성됩니다. 시그마 결합은 원자 궤도 사이의 정면 겹치기 때문에 형성되는 화학 결합의 한 유형입니다. PI 결합은 p 궤도의 겹치기 때문에 형성된다. 알켄에서 이중 결합을 갖는 탄소 원자는 SP 하이브리드 화된다.
alkynes는 하나 이상의 트리플 본드로 구성된 화합물입니다. 트리플 본드는 시그마 본드와 2 개의 PI 결합으로 구성됩니다. 알키네에서 삼중 결합을 갖는 탄소 원자는 SP 혼성화된다. 방향족 화합물은 이중 결합 및 단일 결합으로 구성된 불포화 화합물입니다. 
그림 2 :Alkynes에는 3 중 채권이 있습니다
불포화 화합물은 이중 결합 및 삼중 결합의 존재로 인해 매우 반응성입니다. 탄소 원자 당 수소 원자는 포화 화합물의 수소 원자보다 작다. 그러므로 그들은 불안정합니다. 불포화 화합물은 중합을 겪을 수있다. 불포화 화합물의 중합은 포화 중합체를 만듭니다.
포화 화합물과 불포화 화합물의 차이
정의
포화 화합물 : 포화 화합물은 탄소 탄소 단일 결합 만있는 유기 화합물입니다.
불포화 화합물 : 불포화 화합물은 탄소 원자들 사이에 하나 이상의 이중 결합 또는 삼중 결합을 함유하는 유기 화합물입니다.
화학적 결합
포화 화합물 : 포화 화합물은 탄소 원자 사이에 단일 결합만을 갖는다.
불포화 화합물 : 불포화 화합물은 2 개의 탄소 원자 사이에 적어도 하나의 이중 결합 또는 삼중 결합을 갖는다.
PI 본드
포화 화합물 : 포화 화합물은 탄소 원자 사이에 PI 결합이 없다.
불포화 화합물 : 불포화 화합물은 탄소 원자 사이에 PI 결합을 갖고; 알켄에서 1 개의 PI 결합, 알키 네스의 2 개의 PI 결합.
반응성
포화 화합물 : 포화 화합물은 덜 반응성입니다.
불포화 화합물 : 불포화 화합물은 반응성이 높습니다.
혼성화
포화 화합물 : 포화 화합물의 탄소 원자는 SP 하이브리드 화된다.
불포화 화합물 : 불포화 화합물의 탄소 원자는 SP 또는 SP 하이브리드 화 된 (각각 이중 결합 및 삼중 결합을 갖는 탄소 원자).
분자 당 수소 원자
포화 화합물 : 포화 화합물은 탄소 당 수소 원자가 더 많다.
불포화 화합물 : 불포화 화합물은 포화 화합물과 비교할 때 탄소 원자 당 수소 원자가 적다.
중합
포화 화합물 : 포화 화합물은 중합을 겪지 않습니다.
불포화 화합물 : 불포화 화합물은 중합을 겪습니다.
안정성
포화 화합물 : 포화 화합물은 더 안정적입니다.
불포화 화합물 : 불포화 화합물은 덜 안정적입니다.
예제
포화 화합물 : 포화 화합물에는 알칸과 사이클로 알칸이 포함됩니다.
불포화 화합물 : 불포화 화합물에는 알켄, 알킨 및 방향족 화합물이 포함됩니다.
결론
유기 화합물은 화학적 결합에 따라 포화되거나 불포화 될 수 있습니다. 포화 화합물은 불포화 화합물보다 안정적입니다. 포화 화합물과 불포화 화합물의 주요 차이점은 포화 화합물은 탄소-탄소 단일 결합 만 있고 불포화는 탄소-탄소 이중 결합 및 삼중 결합을 갖는다는 것입니다.
참조 :
1.“포화 대 불모화 탄화수소.” 소프트 스쿨, 여기에서 구할 수 있습니다.
2.“탄화수소의 구조와 명명법.” Purdue, 여기에서 구할 수 있습니다.
이미지 제공 :
1. Commons Wikimedia
2를 통한 "Cyclopropane-2D"(공개 도메인) FVASCONCELLOS 20:06, 2008 년 1 월 8 일 (UTC). drbob의 원본 이미지 (Talk · Contribs). -en







