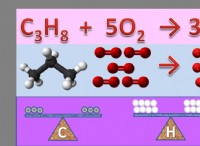
설명 :
* 원자가 생성되거나 파괴되지 않습니다 : 화학 반응은 생성이나 파괴가 아니라 원자의 재 배열을 포함합니다.
* 질량은 보존됩니다 : 원자가 단지 재 배열되기 때문에, 반응물에서 원자의 총 질량은 생성물의 원자의 총 질량과 동일해야한다. 이것은 시스템의 질량이 반응 내내 일정하게 유지됨을 의미합니다.
* 질량이 손실되거나 얻어지지 않습니다 : 반응이 가스를 생성하더라도 가스에는 여전히 질량이 있습니다. 예를 들어, 나무를 태우면 사라지는 것처럼 보이지만 나무 덩어리는 재, 연기 및 가스로 변환됩니다. 제품의 총 질량 (재, 연기 및 가스)은 목재의 초기 질량과 같습니다.
예 :
1. 메탄의 연소 :
- 메탄 (CH4)은 산소 (O2)와 반응하여 이산화탄소 (CO2) 및 물 (H2O)을 생성합니다.
- 반응 전 메탄과 산소의 질량은 이산화탄소 및 물의 질량과 같습니다.
2. 염화나트륨의 형성 :
- 나트륨 (NA)은 염소 (CL2)와 반응하여 염화나트륨 (NaCl)을 형성합니다.
- 반응 전에 나트륨과 염소의 총 질량은 생성 된 염화나트륨의 질량과 같습니다.
시사점 :
* 균형 화학 방정식 : 질량 보존 법칙은 화학 방정식의 균형을 맞추는 데 필수적입니다. 방정식의 양쪽에 각 유형의 원자가 동일한 수를 보장함으로써 질량이 보존되도록 보장합니다.
* 정량 분석 : 질량이 보존된다는 것을 알면 하나 이상의 구성 요소의 질량을 아는 한 반응에서 반응물 또는 생성물의 양을 계산할 수 있습니다.
* 화학 공정 이해 : 질량 보존 법칙은 화학적 변화가 원자를 생성하거나 파괴하지 않는 재배치를 포함한다는 것을 이해하는 데 도움이됩니다. 이것은 환경 화학 및 산업 공정에 영향을 미칩니다.
중요한 참고 :
질량 보존 법칙은 원자력이 아닌 화학 반응에 적용됩니다. 원자 반응에서, 소량의 질량은 에너지로 전환 될 수있다 (아인슈타인의 유명한 방정식 E =mc²에 의해 설명됨).