주요 차이 - 전기 음성 대 전자 친화도
전자는 원자의 아 원자 입자입니다. 모든 물질은 원자로 구성되기 때문에 전자는 어디에서나 발견됩니다. 그러나, 전자는 전자의 교환이 이들 반응에서 반응물과 생성물의 유일한 차이이기 때문에 일부 화학 반응에서 매우 중요하다. 전기 음성 및 전자 친화도는 전자의 존재로 인한 요소의 거동을 설명하는 두 가지 용어입니다. 전기 음성 성과 전자 친화력의 주요 차이점은 전기 음성 성이 전자를 유치하는 원자가의 능력이라는 것입니다 외부에서 전자 친화력은 원자가 전자를 얻을 때 방출되는 에너지의 양입니다.
주요 영역을 다루었습니다
1. 전기성이란 무엇입니까
- 정의, 측정 단위, 원자 번호와의 관계, 본딩
2. 전자 친화력이란?
- 정의, 측정 단위, 원자 번호와의 관계
3. 전기 음성 성과 전자 친화력의 차이점은 무엇입니까
- 주요 차이점 비교
주요 용어 :원자, 전자, 전자 친화력, 전기 음성 성, 흡열 반응, 발열 반응, 폴링 스케일

전기 음성
전기성은 외부에서 전자를 끌어들이는 원자의 능력입니다. 이것은 원자의 질적 특성이며, 각 요소에서 원자의 전기성을 비교하기 위해 상대적인 전기 음성 값이 상상하는 스케일이 사용됩니다. 이 척도는“ Pauling Scale 이라고합니다 .” 이 척도에 따르면, 원자가 가질 수있는 가장 높은 전기 음성 값은 4.0입니다. 다른 원자의 전기성은 전자를 유치하는 능력을 고려할 때 가치가 부여됩니다.
전기성은 요소의 원자 번호와 원자의 크기에 따라 다릅니다. 주기율표를 고려할 때 불소 (F)는 작은 원자이고 원자가 전자는 핵 근처에 있기 때문에 전기 음성에 대한 값 4.0을 제공합니다. 따라서 외부에서 전자를 쉽게 끌어들일 수 있습니다. 또한, 불소의 원자 수는 9이고; 옥트 규칙에 순종하기 위해 하나 이상의 전자에 대한 빈 궤도가 있습니다. 따라서 불소는 외부에서 전자를 쉽게 끌어냅니다.
전기 음성은 두 원자 사이의 결합이 극성이됩니다. 하나의 원자가 다른 원자보다 전기 음성 인 경우, 더 높은 전기성이있는 원자는 결합의 전자를 유치 할 수 있습니다. 이로 인해 다른 원자는 주변의 전자 부족으로 인해 부분 양전하가 발생합니다. 따라서, 전기 음성 성은 화학 결합을 극성 공유, 비극성 공유 및 이온 결합으로 분류하는 열쇠이다. 이온 성 결합은 두 원자 사이에서 발생하는 반면, 공유 결합은 원자들 사이의 전기 음성 성의 약간의 차이를 가진 원자 사이에 발생하는 반면,
.요소의 전기성은 주기적으로 다릅니다. 주기율의 요소 테이블은 전기 음성 값에 따라 요소의 더 나은 배열을 가지고 있습니다.
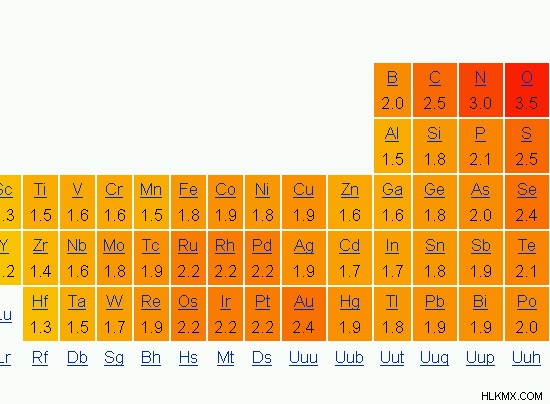
그림 1 :요소의 전기 음성과 함께주기적인 요소 테이블
주기 테이블의주기를 고려할 때 각 요소의 원자 크기는 기간의 왼쪽에서 오른쪽으로 감소합니다. 이는 원자가 쉘에 존재하는 전자의 수와 핵에 양성자의 수가 증가하기 때문에 전자와 핵 사이의 인력이 점차 증가하기 때문이다. 따라서, 핵에서 나오는 매력이 증가하기 때문에 전기 음성도 같은 기간에 따라 증가된다. 그런 다음 원자는 외부에서 전자를 쉽게 끌어들일 수 있습니다.
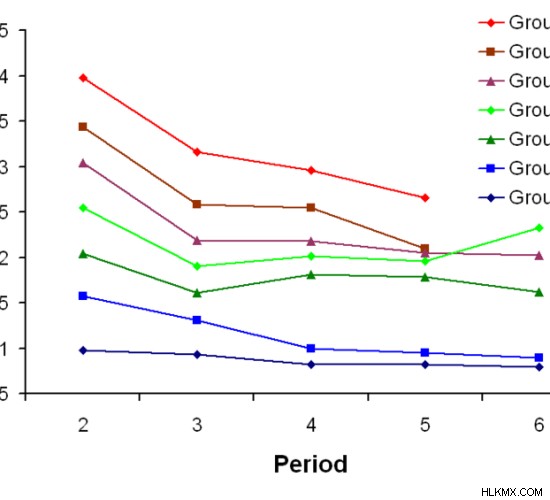
그림 02 :각 그룹의 상단에서 하단으로 전기 음성 (xp)
그룹 17은 각 기간의 가장 작은 원자를 가지므로 전기성이 가장 높습니다. 그러나 궤도의 수가 증가함에 따라 원자 크기가 그룹을 낮추기 때문에 전기 음성 성이 그룹을 감소시킵니다.
전자 친화력이란?
전자 친화력은 중성 원자 또는 분자 (기체 상)가 외부에서 전자를 얻을 때 방출되는 에너지의 양입니다. 이 전자 첨가는 음으로 하전 된 화학 종의 형성을 유발합니다. 이것은 다음과 같이 기호로 표시 될 수 있습니다.
x +e → x +에너지
전자를 중성 원자 또는 분자에 추가하면 에너지를 방출합니다. 이것을 발열 반응 이라고합니다 . 이 반응은 음성 이온을 초래합니다. 그러나 다른 전자 가이 음의 이온에 첨가 될 경우, 그 반응을 진행하기 위해 에너지가 제공되어야한다. 들어오는 전자가 다른 전자에 의해 반발되기 때문입니다. 이 현상을 흡열 반응 이라고합니다 .
따라서 첫 번째 전자 친화력은 음수 값이고 동일한 종의 두 번째 전자 친화도 값은 양수 값입니다.
첫 번째 전자 친화력 :x (g) +e → x (g)
두 번째 전자 친화력 :x (g) +e → x (g)
전기 음성과 동일 한 전자 친화력은 주기율표에서 주기적 변화를 보여줍니다. 들어오는 전자가 원자의 가장 바깥 쪽 궤도에 첨가되기 때문입니다. 주기율표의 요소는 원자 번호의 오름차순 순서에 따라 배열됩니다. 원자 수가 증가하면 가장 바깥 쪽 궤도에있는 전자의 수가 증가합니다.
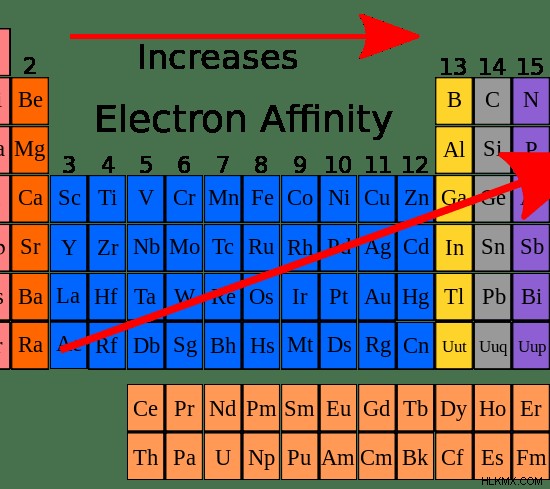
그림 3 :기간에 따라 전자 친화력을 증가시키는 일반적인 패턴
일반적으로 전자 친화력은 전자의 수가 기간에 따라 증가하기 때문에 왼쪽에서 오른쪽으로 증가해야합니다. 따라서 새로운 전자를 추가하기가 어렵습니다. 실험적으로 분석 할 때, 전자 친화도 값은 점진적인 증가를 나타내는 패턴이 아닌 지그재그 패턴을 나타냅니다.
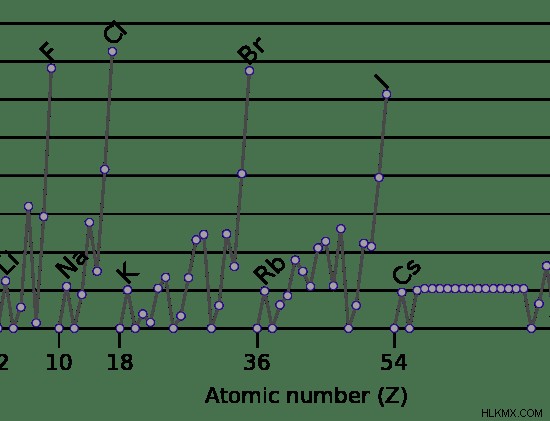
그림 4 :요소의 전자 친화력의 변형
위의 이미지는 리튬 (li)에서 시작하는 기간이 전자 친화력의 점진적인 증가보다는 다양한 패턴을 보여줍니다. 베릴륨 (BE)은 주기율표에서 리튬 (LI) 이후에 나오지만 베릴륨의 전자 친화력은 리튬보다 낮습니다. 이것은 들어오는 전자가 단일 전자가 이미 존재하는 리튬의 궤도로 가져 가기 때문입니다. 이 전자는 들어오는 전자를 격퇴 할 수있어 전자 친화력이 높을 수 있습니다. 그러나 베릴륨에서 들어오는 전자는 반발이 존재하지 않는 유리 P 궤도에 채워진다. 따라서 전자 친화도는 약간 더 적은 값을 갖는다.
전기 음성과 전자 친화도의 차이
정의
전기 음성 : 전기 음성 성은 원자가 외부에서 전자를 유치하는 능력입니다.
전자 친화력 : 전자 친화력은 중성 원자 또는 분자 (기체상에서)가 외부에서 전자를 얻을 때 방출되는 에너지의 양입니다.
.자연
전기 음성 : 전기 음성도는 스케일이 속성을 비교하는 데 사용되는 질적 속성입니다.
전자 친화력 : 전자 친화력은 정량적 측정입니다.
측정 단위
전기 음성 : 전기 음성도는 Pauling 단위에서 측정됩니다.
전자 친화력 : 전자 친화력은 EV 또는 KJ/mol.
로부터 측정된다응용
전기 음성 : 단일 원자에 전기 음성이 적용됩니다.
전자 친화력 : 전자 친화력은 원자 또는 분자에 적용될 수 있습니다.
결론
전기 음성 성과 전자 친화력의 주요 차이점은 전기 음성 성이 외부에서 전자를 끌어들이는 원자가 전자 친화력이 전자를 얻을 때 방출되는 에너지의 양이라는 것입니다.
.






